题目内容
(1)在标准状况下质量相等的NH3和H2S两种气体的体积比为 ,原子个数比为 .
(2)在36g水和20g重水(2H2O)中,分别加入足量的金属钠,在相同条件下产生的气体体积比为 ,产生的气体质量比为 .
(2)在36g水和20g重水(2H2O)中,分别加入足量的金属钠,在相同条件下产生的气体体积比为
考点:物质的量的相关计算
专题:计算题
分析:(1)同温同压下,气体摩尔体积相等,根据V=
×Vm计算其体积之比,根据N=
×NA结合分子构成计算原子个数之比;
(2)根据发生的化学反应为2Na+2D2O═2NaOD+D2↑、2Na+2H2O═2NaOH+H2↑,计算出产生氢气的物质的量,进而算出体积之比和质量之比.
| m |
| M |
| m |
| M |
(2)根据发生的化学反应为2Na+2D2O═2NaOD+D2↑、2Na+2H2O═2NaOH+H2↑,计算出产生氢气的物质的量,进而算出体积之比和质量之比.
解答:
解:同温同压下,气体摩尔体积相等,根据V=
×Vm计算其体积之比,同质量的NH3和H2S气体的体积比为其摩尔质量之比的反比=34g/mol:17g/mol=2:1,
根据N=
×NA结合分子构成计算原子个数之比;
其分子数之比等于其摩尔质量的反比=34g/mol:17g/mol=2:1,结合分子构成知,其原子个数之比为2×4:1×3=8:3,
故答案为:2:1;8:3;
(2)36g水的物质的量为:
=2mol,20g重水的物质的量为:
=1mol
由2Na+2D2O═2NaOD+D2↑、2Na+2H2O═2NaOH+H2↑可知,与足量的钠反应生成氢气的物质的量分别为1mol、0.5mol,物质的量之比为2:1,即体积之比也为2:1;
产生氢气的质量之比为:1mol×2g/mol:0.5mol×4g/mol=1:1
故答案为:2:1;1:1.
| m |
| M |
根据N=
| m |
| M |
其分子数之比等于其摩尔质量的反比=34g/mol:17g/mol=2:1,结合分子构成知,其原子个数之比为2×4:1×3=8:3,
故答案为:2:1;8:3;
(2)36g水的物质的量为:
| 36g |
| 18g/mol |
| 20g |
| 20g/mol |
由2Na+2D2O═2NaOD+D2↑、2Na+2H2O═2NaOH+H2↑可知,与足量的钠反应生成氢气的物质的量分别为1mol、0.5mol,物质的量之比为2:1,即体积之比也为2:1;
产生氢气的质量之比为:1mol×2g/mol:0.5mol×4g/mol=1:1
故答案为:2:1;1:1.
点评:本题考查了阿伏伽德罗定律及其推论,明确各个物理量之间的关系是解本题关键,根据基本公式来分析解答即可,题目难度不大.本题考查钠与水的反应及D、H的摩尔质量的有关计算,明确发生的化学反应及物质的量的简单计算即可解答,题目难度不大,注意D、H的摩尔质量不同.

练习册系列答案
相关题目
下列离子化合物中,阴、阳离子电子层结构相同的是( )
| A、氧化镁 | B、氯化钠 |
| C、溴化钠 | D、氯化镁 |
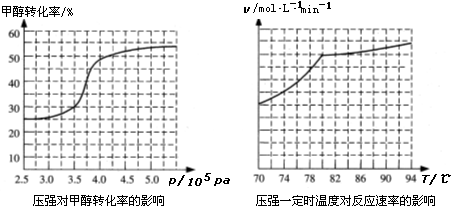
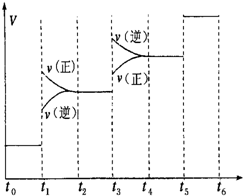 氢气是一种新型的绿色能源,又是一种重要的化工原料.
氢气是一种新型的绿色能源,又是一种重要的化工原料.