题目内容
下列离子方程式一定不正确的是( )
| A、向NH4Fe(SO4)2溶液中加入过量Ba(OH)2溶液:2NH4++Fe3++2SO42-+2Ba2++5OH-=2BaSO4↓+Fe(OH)3↓+2NH3?H2O |
| B、向NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| C、向Na2CO3溶液中加入FeCl3溶液:Fe3++3CO32-+3H2O=Fe(OH)3↓+3HCO3- |
| D、Na2SO3溶液在空气中变质:2SO32-+O2=2SO42- |
考点:离子方程式的书写
专题:
分析:A.不符合铵根离子与铁离子的配比;
B.反应生成沉淀和碳酸钠;
C.相互促进水解生成沉淀和碳酸氢根离子;
D.变质被氧化为硫酸钠.
B.反应生成沉淀和碳酸钠;
C.相互促进水解生成沉淀和碳酸氢根离子;
D.变质被氧化为硫酸钠.
解答:
解:A.向NH4Fe(SO4)2溶液中加入过量Ba(OH)2溶液的离子反应为NH4++Fe3++2SO42-+2Ba2++4OH-=2BaSO4↓+Fe(OH)3↓+NH3?H2O,故A错误;
B.向NaAlO2溶液中通入少量CO2的离子反应为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,故B正确;
C.向Na2CO3溶液中加入FeCl3溶液的离子反应为Fe3++3CO32-+3H2O=Fe(OH)3↓+3HCO3-,故C正确;
D.Na2SO3溶液在空气中变质的离子反应为2SO32-+O2=2SO42-,故D正确;
故选A.
B.向NaAlO2溶液中通入少量CO2的离子反应为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,故B正确;
C.向Na2CO3溶液中加入FeCl3溶液的离子反应为Fe3++3CO32-+3H2O=Fe(OH)3↓+3HCO3-,故C正确;
D.Na2SO3溶液在空气中变质的离子反应为2SO32-+O2=2SO42-,故D正确;
故选A.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应考查,注意C中水解时氯化铁少量,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知Cu+2Fe3+═Cu2++2Fe2+,Zn+2Fe3+═2Fe2++Zn2+.现把等物质的量的CuSO4、FeCl3和Zn置于水中充分反应,反应容器中所得离子除SO42-和Cl-外还含有( )
| A、Zn2+ Cu Fe3+ |
| B、Zn Cu2+ Fe3+ |
| C、Zn2+ Cu Cu2+ Fe2+ |
| D、Zn2+ Cu2+ Fe Fe2+ |
下列说法正确的是( )
| A、硫酸和磷酸的摩尔质量相等 |
| B、18 g水中含有1 molH |
| C、O2的摩尔质量(单位是g?mol-1)在数值上等于其相对分子质量 |
| D、1 mol CO的质量是28 g?mol-1 |
能正确表示下列化学反应的离子方程式是( )
| A、用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32- |
| B、SO2通入到碘水中:SO2+I2+2H2O=2HI+2H++SO42- |
| C、硫化钠溶于水中:S2-+2H2O=H2S↑+2OH- |
| D、碳酸镁溶于硝酸中:CO32-+2H+=H2O+CO2↑ |
下列说法正确的是( )
| A、SO2、SiO2、NO2均为酸性氧化物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、二氧化碳、冰醋酸、四氯化碳均为非电解质 |
| D、福尔马林、水玻璃、氨水均为混合物 |
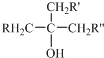 中的-OH不能被氧化.
中的-OH不能被氧化.