题目内容
某强酸性溶液X可能含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42、Cl、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:
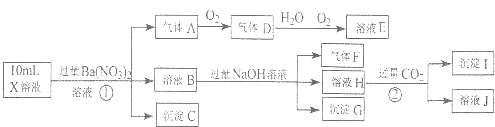
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H-外还肯定含有的离子是 ,不能确定是否含有的离子是 ,若要确定该离子(若不止一种,可任选一种)溶液X中不 存在,最可靠的化学方法是
(2)沉淀I的化学式为
(3)写出反应①生成A的离子方程式
(4)通常可以利用KClO在一定条件下氧化C来制备一种新型、高效、多功能水处理剂K2FeO4,请写出制备过程中的离子方程式
(5)假设测得A、F、I均为0.10mol,10mLX溶液n(H+)=0.45mol,沉淀C物质的量为0.75mol,则溶液X中还一定含 ,其物质的量为 .

根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H-外还肯定含有的离子是
(2)沉淀I的化学式为
(3)写出反应①生成A的离子方程式
(4)通常可以利用KClO在一定条件下氧化C来制备一种新型、高效、多功能水处理剂K2FeO4,请写出制备过程中的离子方程式
(5)假设测得A、F、I均为0.10mol,10mLX溶液n(H+)=0.45mol,沉淀C物质的量为0.75mol,则溶液X中还一定含
考点:无机物的推断,常见离子的检验方法
专题:离子反应专题
分析:强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,以此来解答.
解答:
解:强酸性溶液中一定不会存在CO32-和SO32-离子,加入过量硝酸钡生成沉淀,则该沉淀为BaSO4沉淀,说明溶液中含有SO42-离子,生成气体A,A连续氧化生成D和E,则A为NO,D为NO2,E为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体F,则F为NH3,说明溶液中含有NH4+离子,溶液H中溶于CO2气体,生成沉淀I,则I为Al(OH)3,H为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有SO42-离子就一定不含Ba2+离子,不能确定是否含有的离子Fe3+和Cl-,
(1)由上述分析可知,一定含有Al3+、NH4+、Fe2+、SO42-,可能含Fe3+、Cl-,若要确定该离子在溶液X中不存在,最可靠的化学方法是取原溶液少量于试管中,滴加硝酸酸化的硝酸银溶液,若产生白色沉淀则证明存在Cl-,或取原溶液少量于试管中,滴加KSCN溶液,若变红,则证明存在Fe3+(写出一种即可),
故答案为:Al3+、NH4+、Fe2+、SO42-;Fe3+、Cl-;取原溶液少量于试管中,滴加硝酸酸化的硝酸银溶液,若产生白色沉淀则证明存在Cl-,或取原溶液少量于试管中,滴加KSCN溶液,若变红,则证明存在Fe3+(写出一种即可);
(2)根据上面的分析可知,I为Al(OH)3,
故答案为:Al(OH)3;
(3)反应①生成A的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(4)Fe2+离子被氧化为Fe3+离子,加入NaOH溶液后生成G:Fe(OH)3,和次氯酸反应获得高铁酸钾的方程式为3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O,
故答案为:3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O;
(5)A、F、I均为0.1mol,10mLX溶液中n(H+)=0.45mol,根据反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,可知亚铁离子为0.3mol,根据溶液电中性可知:n(H+)+2n(Fe2+)+3n(Al3+)+n(NH4+)=2n(SO42-),n(SO42-)=
=0.725mol,当沉淀C物质的量为0.75mol时一定含有Fe3+离子,另外溶液中还可能含有Cl-离子,所以其物质的量为≥(0.75-0.725)×
=
,
故答案为:Fe3+;≥
.
(1)由上述分析可知,一定含有Al3+、NH4+、Fe2+、SO42-,可能含Fe3+、Cl-,若要确定该离子在溶液X中不存在,最可靠的化学方法是取原溶液少量于试管中,滴加硝酸酸化的硝酸银溶液,若产生白色沉淀则证明存在Cl-,或取原溶液少量于试管中,滴加KSCN溶液,若变红,则证明存在Fe3+(写出一种即可),
故答案为:Al3+、NH4+、Fe2+、SO42-;Fe3+、Cl-;取原溶液少量于试管中,滴加硝酸酸化的硝酸银溶液,若产生白色沉淀则证明存在Cl-,或取原溶液少量于试管中,滴加KSCN溶液,若变红,则证明存在Fe3+(写出一种即可);
(2)根据上面的分析可知,I为Al(OH)3,
故答案为:Al(OH)3;
(3)反应①生成A的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(4)Fe2+离子被氧化为Fe3+离子,加入NaOH溶液后生成G:Fe(OH)3,和次氯酸反应获得高铁酸钾的方程式为3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O,
故答案为:3ClO-+2Fe(OH)3+4OH-═3Cl-+2FeO42-+5H2O;
(5)A、F、I均为0.1mol,10mLX溶液中n(H+)=0.45mol,根据反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,可知亚铁离子为0.3mol,根据溶液电中性可知:n(H+)+2n(Fe2+)+3n(Al3+)+n(NH4+)=2n(SO42-),n(SO42-)=
| 0.45+2×0.3+3×0.1+0.1 |
| 2 |
| 2 |
| 3 |
| 0.05 |
| 3 |
故答案为:Fe3+;≥
| 0.05 |
| 3 |
点评:本题考查离子组推断题,题目具有一定难度,本题解答时一定要紧扣反应现象,推断各离子存在的可能性,本题易错点为(5)题,注意溶液电中性的利用.

练习册系列答案
相关题目
如图为短周期的一部分,推断关于Y、Z、M说法正确的是( )


| A、非金属性:Y>Z>M |
| B、M2是由非极性共价键构成的分子 |
| C、原子半径:M>Z>Y |
| D、M单质常温下为无色气体 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示,下列说法不正确的是( )


| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是蔗糖溶液 |
| C、利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol |
| D、途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
检验SO2气体中是否存在CO2气体,应采用的方法是( )
| A、通过澄清石灰水 |
| B、先通过小苏打(NaHCO3)溶液,再通过石灰水 |
| C、先通过足量酸性高锰酸钾溶液,再通过石灰水 |
| D、通过品红溶液 |
 25°C时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25°C时,取浓度均为0.1mol?L-1的醋酸溶液和氨水溶液各20mL,分别用0.1mol?L-1NaOH溶液、0.1mol?L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A、曲线I中滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B、曲线I中滴加溶液到25 mL时:c(NH4+)>c(C1-)>c(H+)>c(OH-) |
| C、曲线II中滴加溶液在10 mL~25 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| D、曲线II中滴加溶液到10mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
下列物质的分子内,存在非极性键的是( )
| A、CH4 |
| B、O2 |
| C、Na2O2 |
| D、NH3 |
下列有机化合物中,其核磁共振氢谱图中不可能只出现一个峰的是( )
| A、C2H6 |
| B、C3H8 |
| C、C2H6O |
| D、C5H12 |

 系统命名为
系统命名为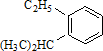 的炔烃的结构简式
的炔烃的结构简式