题目内容
 工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇.如图是实验室中模拟工业原理制取无水乙醇的装置.
工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇.如图是实验室中模拟工业原理制取无水乙醇的装置.回答下列问题:
(1)指出图中的三处错误:
(2)在除去工业酒精中的水时,下列做法不可取的是
A.加入过量的生石灰后过滤
B.加入过量的生石灰后蒸馏
C.加入过量的生石灰后分液
(3)由(2)可知除去工业酒精中的水的原理是(用化学方程式表示)
(4)装置中仪器A、B、C的名称分别是A
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片)的作用是
考点:蒸馏与分馏
专题:实验题
分析:(1)仔细观察制取无水乙醇的装置图,可知给烧瓶加热未垫石棉网,温度计的水银球不应插入溶液中,冷却水的方向接反了;
(2)加入过量的生石灰后,形成的乙醇、Ca(OH)2混合溶液不分层,不能用分液的方法分离;
(3)生石灰与水反应,可以除去工业酒精中的水,CaO+H2O═Ca(OH)2;
(4)由装置图可知,仪器A是温度计;仪器B是蒸馏烧瓶;仪器C是冷凝管;
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片),可以防止暴沸.
(2)加入过量的生石灰后,形成的乙醇、Ca(OH)2混合溶液不分层,不能用分液的方法分离;
(3)生石灰与水反应,可以除去工业酒精中的水,CaO+H2O═Ca(OH)2;
(4)由装置图可知,仪器A是温度计;仪器B是蒸馏烧瓶;仪器C是冷凝管;
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片),可以防止暴沸.
解答:
解:(1)仔细观察制取无水乙醇的装置图,可知给烧瓶加热未垫石棉网,温度计的水银球不应插入溶液中,冷却水的方向接反了;
故答案为:给烧瓶加热未垫石棉网;温度计的水银球插入溶液中;冷却水的方向接反了;
(2)加入过量的生石灰后,形成的乙醇、Ca(OH)2混合溶液不分层,不能用分液的方法分离,故答案为:C
(3)生石灰与水反应,可以除去工业酒精中的水,CaO+H2O═Ca(OH)2;故答案为:CaO+H2O═Ca(OH)2;
(4)由装置图可知,仪器A是温度计;仪器B是蒸馏烧瓶;仪器C是冷凝管;故答案为:温度计;蒸馏烧瓶;冷凝管;
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片),可以防止暴沸;故答案为:防止暴沸.
故答案为:给烧瓶加热未垫石棉网;温度计的水银球插入溶液中;冷却水的方向接反了;
(2)加入过量的生石灰后,形成的乙醇、Ca(OH)2混合溶液不分层,不能用分液的方法分离,故答案为:C
(3)生石灰与水反应,可以除去工业酒精中的水,CaO+H2O═Ca(OH)2;故答案为:CaO+H2O═Ca(OH)2;
(4)由装置图可知,仪器A是温度计;仪器B是蒸馏烧瓶;仪器C是冷凝管;故答案为:温度计;蒸馏烧瓶;冷凝管;
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片),可以防止暴沸;故答案为:防止暴沸.
点评:本题考查有机物的性质及实验,涉及知识点较多,综合性强,较好的考查学生分析解答问题的能力,题目难度中等.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
已知四种盐的溶解度(S)曲线如图所示,下列说法不正确的是( )


| A、将NaCl溶液蒸干可得NaCl固体 |
| B、将MgCl2溶液蒸干可得MgCl2固体 |
| C、可用MgCl2和NaClO3制备Mg(ClO3)2 |
| D、Mg(ClO3)2中混有少量NaCl杂质,可用重结晶法提纯 |
下列说法正确的是( )
| A、用渗析法分离NaCl溶液和淀粉胶体 |
| B、工业制硫酸的吸收塔中用水吸收SO3 |
| C、加足量的稀盐酸可除去BaCO 3 固体中的少量的BaSO4 |
| D、向硝酸银溶液中逐滴加入稀氨水至白色沉淀恰好溶解,即得银氨溶液 |
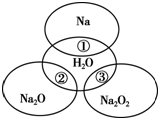 如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、Na2O2中阴阳离子数目之比为1:1 |
| B、反应①的离子方程式为Na+2H2O═Na++2OH-+H2↑ |
| C、反应③最多能转移0.1 mol电子 |
| D、①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③ |
APEC会址选择在雁栖湖作为主会场是为了彰显绿色环保的理念,为此要大力开发低碳技术,推广高效节能技术,积极发展新能源和可再生能源.下列有关做法与此不相符的是( )
| A、在西部和沿海地区兴建风力发电站,解决能源问题 |
| B、回收废弃的饮料包装纸,制作成公园内的休闲长椅 |
| C、大力开发丰富的煤炭资源,减少对石油的依赖 |
| D、鼓励购买小排量汽车,推广电动、混合动力汽车 |
下列溶液肯定呈酸性的是( )
| A、含H+的溶液 |
| B、能使酚酞显无色的溶液 |
| C、PH<7的溶液 |
| D、[H+]>[OH-]的溶液 |
 (X为卤原子)
(X为卤原子)