题目内容
某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案.请你帮助他们完成有关实验项目:
(1)有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性.该原理的离子方程式为 .
(2)有人结合上述(1)的实验并利用Fe、Cu作电极设计成原电池,以确定它们的活动性.试画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式.
正极反应式: .
负极反应式: .
(3)结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同): ,用离子方程式表示其反应原理: .
(1)有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性.该原理的离子方程式为
(2)有人结合上述(1)的实验并利用Fe、Cu作电极设计成原电池,以确定它们的活动性.试画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式.
正极反应式:
负极反应式:
(3)结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同):
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)根据铁与酸的反应分析并写出离子方程式;
(2)利用Fe、Cu作电极设计成原电池,因铁比铜活泼,负极为铁,正极为铜,电解质溶液可为酸或铜盐溶液;
(3)根据铁、铜之间的置换反应设计.
(2)利用Fe、Cu作电极设计成原电池,因铁比铜活泼,负极为铁,正极为铜,电解质溶液可为酸或铜盐溶液;
(3)根据铁、铜之间的置换反应设计.
解答:
解:(1)铁与稀硫酸反应生成硫酸亚铁和氢气,离子方程式为Fe+2H+═Fe2++H2↑,
故答案为:Fe+2H+═Fe2++H2↑;
(2)利用Fe、Cu作电极设计成原电池,因铁比铜活泼,负极为铁,正极为铜,电解质溶液可为酸或铜盐溶液,可设计装置图为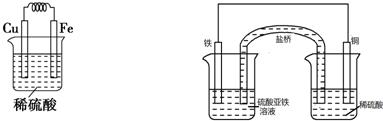 ,负极铁被氧化生成Fe2+,正极H+被还原生成H2,正极反应为2H++2e-→H2↑,负极反应为
,负极铁被氧化生成Fe2+,正极H+被还原生成H2,正极反应为2H++2e-→H2↑,负极反应为
Fe=Fe2++2e-,
故答案为: ;2H++2e-=H2↑;Fe=Fe2++2e-;
;2H++2e-=H2↑;Fe=Fe2++2e-;
(3)根据铁和铜的置换反应设计,设计方法如下:将铁片置于CuSO4溶液中,一段时间后观察Fe表面有红色的金属铜析出,即可以证明金属铁的活泼性强于金属铜的,反应原理为铁和铜离子发生氧化还原反应生成铜和二价铁离子,反应的离子方程式为Fe+Cu2+═Fe2++Cu,
故答案为:取无锈铁棒插入CuSO4溶液,若铁棒表面覆盖一层铜,说明Fe比Cu活动性强;Fe+Cu2+═Cu+Fe2+.
故答案为:Fe+2H+═Fe2++H2↑;
(2)利用Fe、Cu作电极设计成原电池,因铁比铜活泼,负极为铁,正极为铜,电解质溶液可为酸或铜盐溶液,可设计装置图为
 ,负极铁被氧化生成Fe2+,正极H+被还原生成H2,正极反应为2H++2e-→H2↑,负极反应为
,负极铁被氧化生成Fe2+,正极H+被还原生成H2,正极反应为2H++2e-→H2↑,负极反应为Fe=Fe2++2e-,
故答案为:
 ;2H++2e-=H2↑;Fe=Fe2++2e-;
;2H++2e-=H2↑;Fe=Fe2++2e-;(3)根据铁和铜的置换反应设计,设计方法如下:将铁片置于CuSO4溶液中,一段时间后观察Fe表面有红色的金属铜析出,即可以证明金属铁的活泼性强于金属铜的,反应原理为铁和铜离子发生氧化还原反应生成铜和二价铁离子,反应的离子方程式为Fe+Cu2+═Fe2++Cu,
故答案为:取无锈铁棒插入CuSO4溶液,若铁棒表面覆盖一层铜,说明Fe比Cu活动性强;Fe+Cu2+═Cu+Fe2+.
点评:本题以原电池工作原理为载体判断金属的活泼性,注意在原电池中不能仅仅根据电极的正负极判断金属的活泼性,如:在Mg-Al-NaOH溶液组成的原电池中,镁的金属性大于铝,但镁作正极,铝作负极,题目难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
甲、乙两个烧杯中分别盛有100mL 4.0mol/L的盐酸和100mL 4.0mol/L NaOH溶液,向两个烧杯中均加入5.4g铝粉,在相同状况下产生气体的体积比为( )
| A、1:1 | B、2:3 |
| C、3:2 | D、3:1 |
X、Y、Z是短周期的三种主族元素,在周期表中的位置如图所示,下列说法正确的是( )
| X | |
| Y | Z |
| A、X的气态氢化物热稳定性强于Z的气态氢化物 |
| B、原子半径:X<Y<Z |
| C、若Y的最高正价为+m,则X,Z的最高正价一定为+(m+1) |
| D、Y和Z的最高价氧化物对应水化物酸性Y>Z |
氢硫酸在空气中有如此反应:2H2S+O2═2S↓+2H2O,下列不正确的是( )
| A、属于置换反应 |
| B、还原性:H2O>H2S |
| C、氧化性:O2>S |
| D、酸性:H2S>H2O |
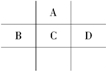 有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同.
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同.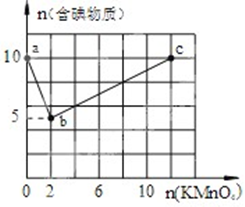 实验一:向含10mol KI的硫酸溶液中逐滴加入高锰酸钾溶液.整个过程中含碘物质与加入高锰酸钾的物质的量的关系如图,已知酸性条件下MnO4-转变为Mn2+.
实验一:向含10mol KI的硫酸溶液中逐滴加入高锰酸钾溶液.整个过程中含碘物质与加入高锰酸钾的物质的量的关系如图,已知酸性条件下MnO4-转变为Mn2+.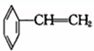 ②
② ③
③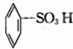 ④
④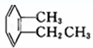 ⑤
⑤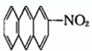
 ⑦
⑦ ⑧CH3CH=CH-COOH⑨
⑧CH3CH=CH-COOH⑨