题目内容
下列事实中,不能证明醋酸是弱酸的是 ( )
| A、醋酸能与大理石反应产生二氧化碳气体 |
| B、pH=3的醋酸溶液稀释100倍后pH<5 |
| C、室温下,醋酸钠溶液的pH>7 |
| D、常温下,0.1 mol?L-1醋酸溶液pH=2.5 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:要证明醋酸为弱酸,可证明存在电离平衡、不能完全电离或从对应的强碱盐溶液呈碱性的角度,以此解答该题.
解答:
解:A.醋酸能够与大理石反应生成二氧化碳,只能说明醋酸的酸性比碳酸强,不能说明醋酸是弱酸,故A选;
B.pH=3的醋酸稀释100倍,其pH<5,说明醋酸中存在电离平衡,可证明醋酸为弱酸,故B不选;
C.测得醋酸钠溶液的pH>7,说明醋酸钠为强碱弱酸盐,水解呈碱性,可证明醋酸为弱酸,故C不选;
D.常温下,测得0.1 mol/L醋酸溶液的pH=2.5,说明醋酸没有完全电离,可证明醋酸为弱酸,故D不选;
故选A.
B.pH=3的醋酸稀释100倍,其pH<5,说明醋酸中存在电离平衡,可证明醋酸为弱酸,故B不选;
C.测得醋酸钠溶液的pH>7,说明醋酸钠为强碱弱酸盐,水解呈碱性,可证明醋酸为弱酸,故C不选;
D.常温下,测得0.1 mol/L醋酸溶液的pH=2.5,说明醋酸没有完全电离,可证明醋酸为弱酸,故D不选;
故选A.
点评:本题考查弱电解质的电离,侧重于弱酸的实验角度的探究,注意把握实验原理和角度,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
| A、950 mL 111.2 g |
| B、500 mL 117.0g |
| C、1000 mL 117.0 g |
| D、1000 mL 111.2 g |
生铁的熔点是1100℃~1200℃,则纯铁的熔点可能是( )
| A、1055℃ |
| B、1100℃ |
| C、1200℃ |
| D、1535℃ |
下列叙述正确的是( )
A、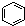 和 和 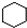 均是芳香烃, 均是芳香烃,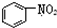 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
| B、分子式为C3H6Cl2的有机物共有5种同分异构体(不考虑立体异构) |
| C、分子式为C4H8有机物最多存在4个C-C单键 |
| D、分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可推测有机物结构简式为C2H5-OH |
某温度时,Kw=1×10-12,下列说法正确的是( )
| A、pH=2的盐酸和pH=12的NaOH溶液等体积混合后,溶液的pH=7 | ||
| B、pH=11的氨水中c(OH-)=0.1mol?L-1 | ||
C、向盐酸中滴加氨水至溶液的pH=6,所得溶液中c(Cl-)>c(N
| ||
| D、将pH=4.5的盐酸稀释100倍后,溶液的pH=6.5 |
光导纤维被认为是20世纪最伟大的发明之一,它使信息高速公路在全球迅猛发展,它的发明者是被誉为“光纤之父”的华人科学家高锟.光导纤维的主要成分是( )
| A、CaCO3 |
| B、SiO2 |
| C、Na2SiO3 |
| D、CaSiO3 |
某无色溶液能与铝反应产生氢气,则在该溶液中不可能大量存在的离子组为( )
| A、Na+、Fe3+、NO3-、Cl |
| B、K+、Na+、Cl-、SO42- |
| C、K+、Ba2+、Br-、Cl- |
| D、NH4+、Na+、CO32-、PO43- |
下列操作中,能使电离平衡H2O?H++OH-向右移动且溶液呈酸性的是( )
| A、向水中加入NaHSO4溶液 |
| B、将水加热到100℃,使pH=6 |
| C、向水中加入Al2(SO4)3固体 |
| D、向水中加入CH3COONa固体 |
下列物质中,既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )
| A、Na2CO3 |
| B、NaHCO3 |
| C、Fe2O3 |
| D、CO2 |