题目内容
(14分)按如图所示装置进行铁和水蒸气反应的实验。

(1)铁粉与水蒸气反应的化学方程式是: ;
(2)为检验生成的气体产物,需从下图选择必要的装置,其正确的连接顺序为(用接口字母表示)
a— ,描述能证明气体产物的实验现象_ ;

(3)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法: ;
(4)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(用化学方程式说明): ;
(5)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是: ;
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有同学设计如下图所示的装置:
通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是________(填序号)。

A.电源中的a为正极,b为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是2H++2e-===H2↑
(每空2分)(1)Fe+4H2O(g) 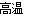 Fe3O4+4H2 (2)a—f—g—b—c—h或a—f—g—c—b—h。
Fe3O4+4H2 (2)a—f—g—b—c—h或a—f—g—c—b—h。
黑色的氧化铜变成红色,白色的无水CuSO4变成蓝色 (3)滴加KSCN溶液,溶液变血红色
(4)2Fe3++Fe=2Fe2+ (5)①4Fe(OH)2+O2+2H2O=4Fe(OH)3 ②BD
【解析】
试题分析:(1)高温下铁与水蒸气反应生成四氧化三铁与氢气,反应的离子方程式为Fe+4H2O(g) 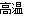 Fe3O4+4H2。
Fe3O4+4H2。
(2)氢气还原氧化铜生成铜和水,利用无水硫酸铜检验生成的水。由于生成的氢气中含有水蒸气,所以需要利用浓硫酸除去氢气中的水蒸气,所以正确的理解顺序为a—f—g—b—c—h或a—f—g—c—b—h。证明有氢气的实验现象是黑色的氧化铜变成红色,白色的无水CuSO4变成蓝色。
(3)检验铁离子一般用KSCN溶液,即取滤液少量与试管中滴加KSCN溶液,溶液变血红色。
(4)反应中铁可能是过量的,过量的铁与铁离子反应生成亚铁离子,即因此2Fe3++Fe=2Fe2+,不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。
(5)①氢氧化亚铁不稳定,易被氧化生成氢氧化铁,反应的方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3;
②A、根据装置图可知,A端有导管,说明有气体产生,因此A端是阴极,溶液中的氢离子放电生成氢气,则电源中的a为负极,b为正极,A不正确;B、氯化钠是强电解质,因此可以用NaCl溶液作为电解液,B正确;C、要得到氢氧化亚铁,则阳极必须是铁,而阴极是惰性电极,C错误;D、阴极发生的反应是2H++2e-===H2↑,D正确,答案选BD。
考点:考查铁与水蒸气反应实验探究、铁离子检验、氢氧化亚铁制备以及电化学的应用等

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项 | 现象或事实 | 解释 |
A. | 用热的纯碱溶液洗去油污 | Na2CO3可直接与油污反应 |
B. | 源白粉在空气中久置变质 | 漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
C. | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
D. | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液中置换出铜 |
 I-+ I2。实验室可以通过氧化还原滴定法测定平衡时I3-的浓度。
I-+ I2。实验室可以通过氧化还原滴定法测定平衡时I3-的浓度。 和CrO
和CrO ,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
 Cr2O
Cr2O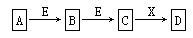

 FeCl3溶液
FeCl3溶液 FeCl3·6H2O晶体
FeCl3·6H2O晶体