题目内容
下列物质不能通过化合反应制取的是( )
| A、Na2SO4 |
| B、Fe(OH)3 |
| C、CH3CHO |
| D、CuS |
考点:铜金属及其重要化合物的主要性质,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:A.过氧化钠和二氧化硫反应生成硫酸钠;
B.氢氧化亚铁、氧气和水反应生成氢氧化铁;
C.乙烯在一定条件下被氧化生成乙醛;
D.Cu在S蒸气中燃烧生成硫化亚铜.
B.氢氧化亚铁、氧气和水反应生成氢氧化铁;
C.乙烯在一定条件下被氧化生成乙醛;
D.Cu在S蒸气中燃烧生成硫化亚铜.
解答:
解:A.Na2O2+SO3=Na2SO4,所以能通过化合反应制取,故A不选;
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以能通过化学反应制取,故B不选;
C.反应2CH2=CH2+O2
2CH3CHO,所以能通过化学反应制取,故C不选;
D.2Cu+S
Cu2S,所以不能通过化学反应制取,故D选;
故选D.
B.4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以能通过化学反应制取,故B不选;
C.反应2CH2=CH2+O2
| 催化剂 |
| △ |
D.2Cu+S
| ||
故选D.
点评:本题考查物质的制取,侧重考查物质的性质及基本概念,明确物质的性质是解本题关键,会正确书写方程式,难点是C选项,题目难度不大.

练习册系列答案
相关题目
某同学通过系列实验,探究Cu及其化合物的性质,操作正确且能达到目的是( )
| A、将铜粉和硫粉混合均匀并加热以制取CuS |
| B、将Cu片放入过量浓硫酸中,一段时间后加水以观察CuSO4溶液的颜色 |
| C、向CuSO4溶液中加入NaOH溶液,过滤洗涤并收集沉淀,加热以制取CuO |
| D、设计Cu-Al-浓硝酸原电池,以证明金属活动性:Cu<Al |
氯气与2,3-二甲基丁烷发生取代反应时,生成的一氯代物有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
现用Pt电极电解1L浓度均为0.1mol/L的HCl、CuSO4的混合液,下列说法正确的是( )
| A、电解开始时,阴极有H2放出 |
| B、电解开始时,阳极上发生:Cu2++2e-═Cu |
| C、当电路中通过电子的量超过0.1mol时,阴极放电的种类将发生变化 |
| D、整个电解过程中,SO42-不参加电极反应 |
海水中有丰富的矿产、能源、药物、水产等化学化工资源,下图是某工厂对海水资源综合利用的示意图.下列有关说法正确的是( )
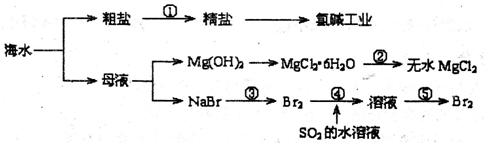

| A、海水中含有丰富的常量元素Mg和Br,以及微量元素I |
| B、流程②为:将MgCl2?6H2O在空气中受热分解制无水MgCl2 |
| C、在流程③④⑤中溴元素均被氧化 |
| D、流程①中欲除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,操作步骤为:依次加入Na2CO3溶液、NaOH溶液、BaCl2溶液,然后过滤,最后加入盐酸 |
将0.1mol?L-1的盐酸逐滴加入体积与物质的量浓度均相等的甲、乙、丙三种溶液中,当溶液呈中性时,消耗盐酸的体积大小顺序为( )
| 甲 | 乙 | 丙 |
| 氨水 | KOH | K2CO3 |
| A、甲>乙>丙 |
| B、乙>甲>丙 |
| C、丙>乙>甲 |
| D、丙>甲>乙 |
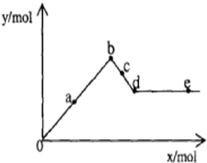 已知Ba(AlO2)2可溶于水.如图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述错误的是( )
已知Ba(AlO2)2可溶于水.如图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述错误的是( )| A、d-e 时溶液中离子的物质的量:Ba2+可能等于AlO2- |
| B、b-c 时溶液中离子的物质的量:AlO2-比Ba2+多 |
| C、a-d 时沉淀的物质的量:Al(OH)3一定小于BaSO4 |
| D、a-b 时沉淀的物质的量:Al(OH)3比BaSO4多 |