题目内容
关注饮用水,保证人民的生活质量.回答下列三个问题:饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O.请回答下列问题:
(1)上述反应中的氧化剂为 .
(2)用单线桥标出上述反应转移的电子总数和方向
(3)当转移1mol电子时,标准状况下产生的N2 体积为 L.
(1)上述反应中的氧化剂为
(2)用单线桥标出上述反应转移的电子总数和方向
(3)当转移1mol电子时,标准状况下产生的N2 体积为
考点:氧化还原反应,氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:反应10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,Al元素化合价升高,被氧化,N元素化合价降低,被还原,结合化合价的变化判断电子的得失以及电子转移的方向和数目;据此分析判断.
解答:
解:(1)反应10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O中,Al元素化合价升高,被氧化,N元素化合价降低,被还原,则NaNO3为氧化剂,
故答案为:NaNO3;
(2)反应中铝失去电子数为10×3,NaNO3得到电子数为6×5,所以用“双线桥法”标明反应中电子转移的方向和数目为: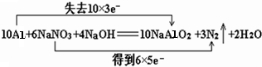 ,
,
故答案为: ;
;
(3)产生1mol气体,则转移的电子的物质的量为1mol×2×(5-0)=10mol,则转移1mol电子是生成0.1mol氮气,即2.24L;
故答案为:2.24.
故答案为:NaNO3;
(2)反应中铝失去电子数为10×3,NaNO3得到电子数为6×5,所以用“双线桥法”标明反应中电子转移的方向和数目为:
 ,
,故答案为:
 ;
;(3)产生1mol气体,则转移的电子的物质的量为1mol×2×(5-0)=10mol,则转移1mol电子是生成0.1mol氮气,即2.24L;
故答案为:2.24.
点评:本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
下列化合物的核磁共振氢谱中出现三个峰的是( )
| A、2,5二甲基己烷 |
| B、3,4二甲基己烷 |
| C、2,3,4三甲基戊烷 |
| D、2,2,3,3四甲基丁烷 |
看电影时,同学们可以看到放映机投射的光柱,这就是气溶胶发生的丁达尔现象.胶体区别于其它分散系的本质特征是( )
| A、胶体的分散质能透过滤纸 |
| B、胶体能产生丁达尔现象 |
| C、胶体的分散质粒子直径在1~100nm之间 |
| D、胶体是纯净物,其它分散系是混合物 |
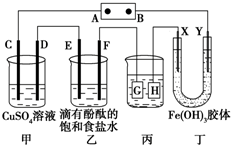 如图所示装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中的溶液都是1mol?L-1 500mL(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答:
如图所示装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中的溶液都是1mol?L-1 500mL(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答: 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: