题目内容
5.A-H等8种物质存在下列转换关系(反应条件,部分产物未标出).已知:A是正盐,B是能使品红溶液褪色的气体,G是红棕色气体.E能使湿润的红色石蕊试纸变蓝.按要求回答: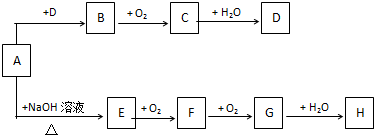
(1)写出下列物质的化学式:A(NH4)2SO3,BSO2,CSO3.
(2)写出下列反应的化学方程式:E→F4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O; G→H3NO2+H2O=2HNO3+NO,H的浓溶液与红热的木炭反应的方程式:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(3)检验A中阳离子的离子方程式:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
分析 A是正盐,与氢氧化钠反应生成的E能使湿润的红色石蕊试纸变蓝,E与氧气连续反应生成G是红棕色气体,则A为铵盐,E是NH3,F是NO,G是NO2,H是HNO3.B是能使品红溶液褪色的气体,结合转化关系可知,B是SO2,A是(NH4)2SO3,C是SO3,D是H2SO4.
解答 解:A是正盐,与氢氧化钠反应生成的E能使湿润的红色石蕊试纸变蓝,E与氧气连续反应生成G是红棕色气体,则A为铵盐,E是NH3,F是NO,G是NO2,H是HNO3.B是能使品红溶液褪色的气体,结合转化关系可知,B是SO2,A是(NH4)2SO3,C是SO3,D是H2SO4.
(1)由上述分析可知,A是(NH4)2SO3,B是SO2,C是SO3,
故答案为:(NH4)2SO3;SO2;SO3;
(2)E→F的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
G→H的化学方程式:3NO2+H2O=2HNO3+NO,
硝酸的浓溶液与红热的木炭反应的方程式:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;3NO2+H2O=2HNO3+NO;C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(3)利用铵盐与碱反应生成碱性气体氨气来检验铵根离子,反应离子方程式:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,
故答案为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
点评 本题考查无机物的推断,物质的颜色及特殊性质是推断突破口,需要学生熟练掌握元素化合物性质,注意掌握常见连续反应与常见离子检验.

| A. | 烧杯中有铜、铁均有 | B. | 烧杯中Fe3+、Cu2+、Fe2+均有 | ||
| C. | 烧杯中Cu和Cu2+均有 | D. | 烧杯中Cu2+、Fe2+、Cu和Fe均有 |
| A. | 钠和氢气分别在氯气中燃烧,都产生白色烟雾 | |
| B. | 铜丝在氯气中燃烧,生成蓝色的氯化铜 | |
| C. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液呈红色 | |
| D. | 氯水中滴入硝酸银溶液会产生白色沉淀 |
 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O.
 有可逆反应A(g)+B(g)?xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变.A、B、C、D物质的量随时间的变化如图所示:
有可逆反应A(g)+B(g)?xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变.A、B、C、D物质的量随时间的变化如图所示: