题目内容
 参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的( )
参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的( )| A、正反应为放热反应 |
| B、加入催化剂,该化学反应的反应热不改变 |
| C、加入催化剂,该化学反应的活化能不改变 |
| D、加入催化剂可增大正反应速率,降低逆反应速率 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:根据图中的数据,可以看出反应物的总能量小于生成物的总能量,可知该反应吸热反应;催化剂与反应热无关,催化剂同等程度改变正逆反应速率;据此即可解答.
解答:
解:A.根据图中的数据,可以看出是反应物的能量小于生成物的能量,则反应是吸热反应,故A错误;
B.催化剂只能改变反应的活化能,不会改变化学反应的反应热,反应热只与反应的始态与终态有关,与反应途径、是否使用催化剂无关,故B正确;
C.催化剂改变反应的活化能,改变反应速率,故C错误;
D.催化剂同等程度改变正逆反应速率,故D错误;
故选B.
B.催化剂只能改变反应的活化能,不会改变化学反应的反应热,反应热只与反应的始态与终态有关,与反应途径、是否使用催化剂无关,故B正确;
C.催化剂改变反应的活化能,改变反应速率,故C错误;
D.催化剂同等程度改变正逆反应速率,故D错误;
故选B.
点评:本题考查吸热反应和放热反应等,注意反应热只与反应的始态与终态有关,与反应途径、是否使用催化剂无关.本题难度不大.

练习册系列答案
相关题目
采用下列装置和操作,能达到实验目的是( )
A、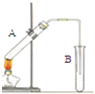 A中为乙醇、醋酸,B中为饱和碳酸钠溶液,制取乙酸乙酯 |
B、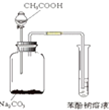 验证醋酸、碳酸、苯酚的酸性强弱 |
C、 用浓硫酸、乙醇共热到约170℃制乙烯 |
D、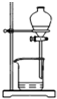 用NaOH溶液除去苯中混有的少量苯酚 |
全钒液流储能电池(VRB)广泛应用于风能、太阳能发电系统的储能系统.电池反应为VO2++V2++2H+
VO2+V3+H2O,下列说法正确的是( )
| 放电 |
| 通电 |
| A、充电时,外接电源的正极与电池上标注“-”的电极连接 |
| B、电池工作时,H+由正极流向负极 |
| C、电池放电时,负极的电极反应为VO2++H2O=VO2++2H++e- |
| D、电池充电时,阴极的电极反应为V3++e-=V2+ |
下列说法或表示法正确的是( )
| A、由C(s,石墨)→C(s,金刚石)△H=+1.9kJ?mol-1可知,石墨比金刚石稳定 |
| B、在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(1)△H=-285.8kJ?mol-1 |
| C、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| D、压缩容器的体积,平衡2SO2+O2?2SO3正向移动,该反应的△H减小 |
下列离子方程式正确的是( )
| A、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、澄清石灰水跟盐酸反应:H++OH-=H2O |
| C、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| D、氯化铁溶液跟铜反应:Fe3++Cu=Fe2++Cu2+ |
水溶液中能大量共存的一组离子是( )
| A、Al3+、Na+、CO32-、NO3- |
| B、Ag+、Cl-、Fe3+、HCO3- |
| C、Fe2+、H+、K+、MnO4- |
| D、Mg2+、Br-、NH4+、SO42- |
下列图示与对应的叙述不相符的是( )

| A、图1说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
| B、向盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系有可能是图2 |
| C、图3表示KNO3的溶解度曲线,图中a点所示的溶液在80℃时不可能存在 |
| D、在体积相同的两个密闭容器中,分别充入等质量的O2和X气体,由图4可确定X可能是CH4 |
X、Y、Z、W是短周期元素,原子序数依次递增.X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14.下列说法正确的是( )
| A、气态氢化物的稳定性:X<Z<W |
| B、Y的阳离子半径比W的阴离子半径小 |
| C、X、Z、W氧化物对应水化物酸性的强弱顺序为Z<X<W |
| D、室温下,含Y元素的盐形成的水溶液其pH<7 |