题目内容
下列方程式书写正确的是( )
| A、向小苏打溶液中加入NaAlO2:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32- |
| B、碳酸氢钠溶液跟过量的饱和石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| C、NaHSO4溶液中滴入少量Ba(OH)2:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| D、200mL2mol/LFeBr2溶液中通入11.2L标况下的Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-? |
考点:离子方程式的书写
专题:离子反应专题
分析:A.促进小苏打的电离生成碳酸钠和氢氧化铝;
B.碳酸氢钠完全反应,生成碳酸钙、水、NaOH;
C.少量Ba(OH)2完全反应,生成硫酸钡、硫酸钠和水;
D.n(FeBr2)=0.4mol,n(Cl2)=0.5mol,由电子守恒可知,亚铁离子全部被氧化,溴离子只有部分氧化.
B.碳酸氢钠完全反应,生成碳酸钙、水、NaOH;
C.少量Ba(OH)2完全反应,生成硫酸钡、硫酸钠和水;
D.n(FeBr2)=0.4mol,n(Cl2)=0.5mol,由电子守恒可知,亚铁离子全部被氧化,溴离子只有部分氧化.
解答:
解:A.促进小苏打的电离生成碳酸钠和氢氧化铝,离子反应为AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-,故A正确;
B.碳酸氢钠完全反应,生成碳酸钙、水、NaOH,离子反应为HCO3-+Ca2++OH-=CaCO3↓+H2O,故B错误;
C.少量Ba(OH)2完全反应,生成硫酸钡、硫酸钠和水,离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故C错误;
D.n(FeBr2)=0.4mol,n(Cl2)=0.5mol,由电子守恒可知,亚铁离子全部被氧化,溴离子只有部分氧化,离子反应为4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl-,故D错误;
故选A.
B.碳酸氢钠完全反应,生成碳酸钙、水、NaOH,离子反应为HCO3-+Ca2++OH-=CaCO3↓+H2O,故B错误;
C.少量Ba(OH)2完全反应,生成硫酸钡、硫酸钠和水,离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故C错误;
D.n(FeBr2)=0.4mol,n(Cl2)=0.5mol,由电子守恒可知,亚铁离子全部被氧化,溴离子只有部分氧化,离子反应为4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl-,故D错误;
故选A.
点评:本题考查离子反应方程式书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、氧化还原反应的离子反应考查,选项AD为解答的难点,题目难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
对于反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
A、K=
| ||
B、K=
| ||
| C、增大c(H2O)或减小c(H2),会使该反应平衡常数减小 | ||
| D、改变反应的温度,平衡常数不一定变化 |
下列推断正确的是( )
| A、Na2O和Na2O2组成元素相同,与CO2反应产物也相同 |
| B、SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 |
| C、NO和NO2的密度均比空气大,都可用向上排空气法收集 |
| D、C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,二者沸点也相近 |
有关实验操作或实验突发事件处理正确的是( )
| A、用10mL量筒量取8.58mL蒸馏水 |
| B、将氢氧化钠固体直接放在称量纸上称量 |
| C、中和滴定时,滴定管用蒸馏水洗净后直接装入标准盐酸溶液 |
| D、不慎将苯酚溶液沾到皮肤上,立即用酒精清洗 |
化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A、航天服材质是由碳化硅、陶瓷和碳纤维等复合而成,它是一种新型无机非金属材料 |
B、 是放射性警示的标志 是放射性警示的标志 |
| C、雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同 |
| D、煤的主要成分为单质碳、苯、二甲苯等,因而可通过煤的干馏将它们分离 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol Na2O2固体中含离子总数为4NA | ||
| B、标准状况下,22.4L己烷中共价键数目为19NA | ||
| C、由乙烯和环己烷组成的混合物28g,含电子数为16NA | ||
D、1L浓度为1mol/L的Na2CO3溶液中含有的
|
若在加入铝粉能放出H2的溶液中,分别加入下列各组离子,可能大量共存的是( )
| A、NH4+ NO3- CO32- Na+ |
| B、Na+ Ba2+ Mg2+ HCO3- |
| C、Cu2+ Fe3+ K+ Cl- |
| D、NO3- K+ AlO2- H+ |
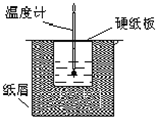 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题: