题目内容
18.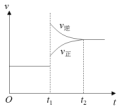 如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )| A. | 使用催化剂 | B. | 升高温度 | C. | 增大压强 | D. | 提高 N2浓度 |
分析 合成氨反应为N2(g)+3H2(g)?2NH3(g)△H<0,由图象可知t1时刻改变外界条件,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡逆向移动,以此解答该题.
解答 解:A.催化剂同等程度改变反应速率,平衡不移动,故A错误;
B.正反应放热,升高温度,正逆反应速率都增大,平衡逆向移动,故B正确;
C.增大压强,平衡正向移动,正反应速率大于逆反应速率,故C错误;
D.提高 N2浓度,平衡正向移动,故D错误.
故选B.
点评 本题考查影响化学平衡的影响因素,为高频考点,侧重考查学生的分析能力,注意把握浓度、催化剂、温度、压强对平衡移动以及反应速率的影响,侧重反应速率图象的分析,明确速率变化程度为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
8.常温下,向1LpH=10的KOH溶液中持续通入CO2,与溶液中水电离出的c(OH-)与通入的CO2的体积(V)关系如图所示.下列叙述不正确的是( )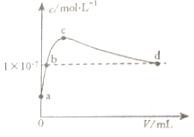

| A. | b点溶液呈中性 | |
| B. | d点溶液中:c(K+)=2c(CO32-)+c(HCO3-) | |
| C. | c点溶液中:2c(H2CO3)+c(H+)+c(HCO3-)=c(OH-) | |
| D. | a点溶液中:水电离出的c(H+)=1×10-10mol•L-1 |
9.向3mol•L-1盐酸中加入打磨后的镁条,一段时间后生成灰白色固体X,并测得反应后溶液pH升高.为确认固体X的成分,过滤洗涤后进行实验:
①向固体X中加入足量硝酸,固体溶解,得到无色溶液,将其分成两等份;
②向其中一份无色溶液中加入足量AgNO3溶液,得到白色沉淀a;
③向另一份无色溶液中加入足量NaOH溶液,得到白色沉淀b.
下列分析不正确的是( )
①向固体X中加入足量硝酸,固体溶解,得到无色溶液,将其分成两等份;
②向其中一份无色溶液中加入足量AgNO3溶液,得到白色沉淀a;
③向另一份无色溶液中加入足量NaOH溶液,得到白色沉淀b.
下列分析不正确的是( )
| A. | 溶液pH升高的主要原因:Mg+2H+═Mg2++H2↑ | |
| B. | 生成沉淀a的离子方程式:Ag++Cl-═AgCl↓ | |
| C. | 沉淀b是Mg(OH)2 | |
| D. | 若a、b的物质的量关系为n(a):n(b)=1:3,则可推知固体X的化学式为Mg3(OH)6Cl |
6.化学与社会、生活密切相关.对下列现象或事实及解释均正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 化石燃料燃烧时采取脱硫措施 | 提高化石燃料的利用率 |
| B | 食品袋中常放有硅胶和铁粉,都能起到干燥的作用 | 二者都有较强的吸水性 |
| C | 高温加热能杀死流感病毒 | 蛋白质受热变性 |
| D | 高铁车厢采用铝合金材料 | 铝和氧气不反应 |
| A. | A | B. | B | C. | C | D. | D |
13.下列有关化学用语表达正确的是( )
| A. | 氟化氢的电子式: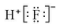 | |
| B. | 氯原子的结构示意图: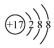 | |
| C. | 丙烯的结构简式:C3H6 | |
| D. | 硫原子的最外层电子排布式:3s23p4 |
3.下列分子中,属干含有极性健的非极性分子的是( )
| A. | H2O | B. | Br2 | C. | CH4 | D. | HCl |
10.醋酸钠中不存在( )
| A. | 离子键 | B. | 极性键 | C. | 非极性键 | D. | 分子间作用力 |
20.钠与铯都是碱金属,下列关于铯及其化合物的叙述中正确的是( )
| A. | 铯的密度比水小,像钠一样浮在水面上 | |
| B. | 铯与水反应十分剧烈,甚至会发生爆炸 | |
| C. | 碳酸铯加热时易分解成二氧化碳和氧化铯 | |
| D. | 氢氧化铯是强碱,其碱性比氢氧化钾弱 |
 创新发展材料技术可推动人类社会进步.
创新发展材料技术可推动人类社会进步.