题目内容
铁是重要的常见金属材料,也是人类较早使用的金属之一,请运用铁及其化合物的知识完成下列问题.
(1)铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入四氧化三铁和铝粉的混合物,用镁条引燃发生反应,写出发生置换反应的化学方程式并用单线桥法标出电子转移方向和数目 ;
(2)向20mL的沸蒸馏水中逐滴滴加5~6滴0.1mol/L的FeCl3溶液,继续煮沸没有观察到透明的红褐色现象,请问此时分散系中粒子直径 1nm(填>、<或=),判断的依据是 ;检验该分散系阳离子的常用方法是 (用离子方程式表示)
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式: .
(4)欲从废腐蚀液中回收铜,并重新获得FeCl3溶液,设计实验方案如图:
请写出上述实验中加入或生成的有关物质的化学式:

① ③ ④ .
(1)铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入四氧化三铁和铝粉的混合物,用镁条引燃发生反应,写出发生置换反应的化学方程式并用单线桥法标出电子转移方向和数目
(2)向20mL的沸蒸馏水中逐滴滴加5~6滴0.1mol/L的FeCl3溶液,继续煮沸没有观察到透明的红褐色现象,请问此时分散系中粒子直径
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(4)欲从废腐蚀液中回收铜,并重新获得FeCl3溶液,设计实验方案如图:
请写出上述实验中加入或生成的有关物质的化学式:

①
考点:铝的化学性质,铁盐和亚铁盐的相互转变,物质的分离、提纯的基本方法选择与应用
专题:元素及其化合物
分析:(1)化合价升高元素失电子,化合价降低元素得电子,化合价升高值=化合价降低值=转移电子数,据此回答;
(2)根据胶体分散系的微粒直径大小范围是1~100nm来回答判断;检验铁离子常用硫氰化钾溶液;
(3)铁离子具有氧化性,能和还原性的物质Cu之间发生反应;
(4)实验的目的是制取FeCl3溶液,借助金属铜和铁的性质差异来除去金属铜,用氯气将氯化亚铁氧化为铁离子,据此回答判断.
(2)根据胶体分散系的微粒直径大小范围是1~100nm来回答判断;检验铁离子常用硫氰化钾溶液;
(3)铁离子具有氧化性,能和还原性的物质Cu之间发生反应;
(4)实验的目的是制取FeCl3溶液,借助金属铜和铁的性质差异来除去金属铜,用氯气将氯化亚铁氧化为铁离子,据此回答判断.
解答:
解:(1)铝热反应中,Al元素化合价升高失电子,Fe元素化合价降低得电子,化合价升高值=化合价降低值=转移电子数=24,即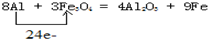 ,故答案为:
,故答案为: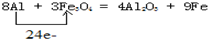 ;
;
(2)向20mL的沸蒸馏水中逐滴滴加5~6滴0.1mol/L的FeCl3溶液,继续煮沸没有观察到透明的红褐色现象,此时得到的分散系属于溶液,分散质微粒直径大小是<1nm,而胶体粒子粒径在1-100nm之间;铁离子遇到硫氰化钾溶液会显红色,反应离子方式为:Fe3++3SCN-═Fe(SCN)3;
故答案为:<1;该实验所用FeCl3 浓度低,没有制备出胶体仍是溶液,故粒子直径<1nm;Fe3++3SCN-═Fe(SCN)3;
(3)铁离子具有氧化性,能和还原性的物质Cu之间发生反应:2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(4)①制取的是氯化铁溶液,金属①是铁;滤液②是氯化亚铁溶液;加入的铁过量,滤渣③是铁和铜;制取的是氯化铁,溶解铁,④加入应该是盐酸;
故答案为:Fe;Fe、Cu;HCl.
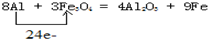 ,故答案为:
,故答案为: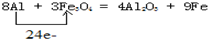 ;
;(2)向20mL的沸蒸馏水中逐滴滴加5~6滴0.1mol/L的FeCl3溶液,继续煮沸没有观察到透明的红褐色现象,此时得到的分散系属于溶液,分散质微粒直径大小是<1nm,而胶体粒子粒径在1-100nm之间;铁离子遇到硫氰化钾溶液会显红色,反应离子方式为:Fe3++3SCN-═Fe(SCN)3;
故答案为:<1;该实验所用FeCl3 浓度低,没有制备出胶体仍是溶液,故粒子直径<1nm;Fe3++3SCN-═Fe(SCN)3;
(3)铁离子具有氧化性,能和还原性的物质Cu之间发生反应:2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(4)①制取的是氯化铁溶液,金属①是铁;滤液②是氯化亚铁溶液;加入的铁过量,滤渣③是铁和铜;制取的是氯化铁,溶解铁,④加入应该是盐酸;
故答案为:Fe;Fe、Cu;HCl.
点评:本题涉及含铁元素的化合物的性质、胶体的制备、氧化还原反应中电子转移等知识,属于综合知识的考查,题目难度中等.

练习册系列答案
相关题目
下列有机反应方程式中,正确的是( )
A、C2H5Br+NaOH
| |||
B、 +3HNO3 +3HNO3
 +3H2O +3H2O | |||
C、 +CH2=CH2 +CH2=CH2
 | |||
D、n +n +n
 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、由水电离的c(H+)=1×l0-12 mol?L-1的溶液中:Ba2+、K+、Cl-、NO
| ||||
B、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO
| ||||
C、无色溶液中:K+、Na+、MnO
| ||||
D、含有大量HCO
|
乙醇分子中的化学键如图.下列关于乙醇在不同的反应中化学键断裂的说法正确的( )


| A、与金属钠反应时,键②断裂 |
| B、与浓硫酸共热至140℃时,键③、⑤断裂 |
| C、在Cu催化下与O2反应时,键①、③断裂 |
| D、与浓硫酸共热至170℃时,键①、②断裂 |
在相同温度和压强下,1mol Ar和1mol NH3具有相同的( )
| A、分子数 | B、质量 |
| C、原子数 | D、体积 |
