题目内容
下列有关金属的说法正确的是( )
| A、金属原子只有还原性,金属阳离子只有氧化性 |
| B、金属单质在常温下都是固体 |
| C、金属阳离子被还原不一定得到金属单质 |
| D、含金属元素的离子都是阳离子 |
考点:金属的通性
专题:几种重要的金属及其化合物
分析:A.金属阳离子可能具有还原性;
B.金属单质Hg常温下为液体;
C.金属阳离子被还原不一定得到金属单质,可能生成较低价态的离子;
D.含有金属元素的离子可能是阴离子.
B.金属单质Hg常温下为液体;
C.金属阳离子被还原不一定得到金属单质,可能生成较低价态的离子;
D.含有金属元素的离子可能是阴离子.
解答:
解:A.金属阳离子可能具有还原性,如Fe 2+,故A错误;
B.金属单质Hg常温下为液体,是唯一的液态金属单质,故B错误;
C.金属阳离子被还原不一定得到金属单质,可能生成较低价态的离子,如2Fe3++Cu=Cu2++2Fe2+,故C正确;
D.含有金属元素的离子可能是阴离子,如AlO2-,故D错误;
故选C.
B.金属单质Hg常温下为液体,是唯一的液态金属单质,故B错误;
C.金属阳离子被还原不一定得到金属单质,可能生成较低价态的离子,如2Fe3++Cu=Cu2++2Fe2+,故C正确;
D.含有金属元素的离子可能是阴离子,如AlO2-,故D错误;
故选C.
点评:本题考查金属的有关知识,涉及氧化还原反应、金属的状态等知识点,熟记规律中的异常现象,题目难度不大.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
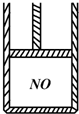 如图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)( )
如图为装有活塞(质量忽略不计)的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度为(提示:不考虑NO转化为NO2的可逆性)( )| A、等于1.369g?L-1 |
| B、等于2.054g?L-1 |
| C、在1.369g?L-1和2.054g?L-1之间 |
| D、在2.054g?L-1和4.108g?L-1之间 |
中学化学教材中,常借助于图象的这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理.下列有关化学图象表现的内容正确的是( )
A、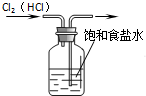 除去Cl2中的HCl杂质 |
B、 稀释浓H2S04 |
C、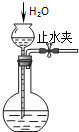 检查装置气密性 |
D、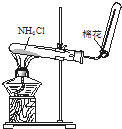 实验室制取NH3 |
下列叙述正确的是( )
| A、1H和3H的质子数相同,它们是同种核素 |
| B、6Li和7Li的质子数相等,电子数也相等 |
| C、14C和14N的质量数相等,它们的中子数相等 |
| D、13C和14C属于同一种元素,它们的质量数相等 |
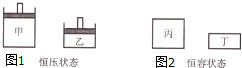 一定条件下存在反应:2SO2(g)+O2(g)?2SO3(g),其正反应放热.图1、图2表示起始时容器甲、丙体积都V,容器乙、丁体积都是
一定条件下存在反应:2SO2(g)+O2(g)?2SO3(g),其正反应放热.图1、图2表示起始时容器甲、丙体积都V,容器乙、丁体积都是| V |
| 2 |
| A、图1达平衡时,浓度c(SO2):甲=乙 |
| B、图1达平衡时,平衡常数K:甲>乙 |
| C、图2达平衡时,所需时间t:丙<丁 |
| D、图2达平衡时,体积分数φ(SO3):丙>丁 |
已知BrCl能发生下列反应:nBrCl+2M=MCln+MBrn(M为+n价的金属元素),BrCI+H20=HCl+HBrO,以下推论正确的是( )
| A、BrCl具有和卤素单质相似的化学性质 |
| B、BrCl和M反应时,BrCl即为氧化剂又为还原剂 |
| C、BrCl和NaOH溶液反应生成NaCI、NaBrO两种盐 |
| D、将BrCl跟FeS04溶液反应.溶液会变成无色 |