题目内容
3.下列说法正确的是( )| A. | 化学反应除了生成新的物质外,只伴随着热量的变化 | |
| B. | 物质燃烧不一定是放热反应,放热的化学反应不需要加热就能发生 | |
| C. | 太阳能、氢能、生物质能属于新能源 | |
| D. | 化石燃料是一次能源,乙醇是不可再生能源 |
分析 A、化学反应在发生物质变化的同时还伴随着能量的变化;
B、反应放热和吸热只决定与反应物和生成物的能量高低,与反应条件无关;
C、太阳能、潮汐能、风能、氢能、生物质能等都是可再生、无污染的新能源;
D、使用完后不可能在短时间内形成,是不可再生能源.
解答 解:A、化学反应在发生物质变化的同时还伴随着能量的变化,其中能量包括热量、光能等能量,故A错误;
B、燃烧都是放热反应,但必须加热到物质的着火点,故B错误;
C、太阳能、氢能、生物质能都属于新能源,故C正确;
D、化石能源使用完后不可能在短时间内形成,是不可再生能源,属于一次能源,乙醇是可再生能源,故D错误.
故选C.
点评 本题考查常见的能量转换形式,以及化学反应中能量变化的原因,可以根据教材知识来回答,较简单.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
14.化学与环境、生活密切相关,下列与化学有关的说法正确的是( )
| A. | 春节燃放爆竹对环境无污染 | |
| B. | “酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | 光化学烟雾的产生与人为排放大气污染物氮氧化物无关 |
11.你认为下列对化学知识概括合理的组合是( )
①金属晶体中存在离子,但却不存在离子键
②原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
③原子晶体硬度一般比分子晶体大,分子晶体熔点不一定比金属晶体低
④固态能导电的一定是金属晶体
⑤NF3的沸点比NH3的沸点低是因为N-F比N-H键的键能小
⑥原子晶体一定由原子构成,由原子构成的晶体不一定是原子晶体
⑦共价化合物中可能含有离子键
⑧金属晶体中简单立方堆积的配位数是8,空间利用率最低.
①金属晶体中存在离子,但却不存在离子键
②原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
③原子晶体硬度一般比分子晶体大,分子晶体熔点不一定比金属晶体低
④固态能导电的一定是金属晶体
⑤NF3的沸点比NH3的沸点低是因为N-F比N-H键的键能小
⑥原子晶体一定由原子构成,由原子构成的晶体不一定是原子晶体
⑦共价化合物中可能含有离子键
⑧金属晶体中简单立方堆积的配位数是8,空间利用率最低.
| A. | 只有②③④ | B. | 只有②③⑦ | C. | 只有①③⑥ | D. | 只有⑤⑥⑧ |
18.某学习小组研究溶液中Fe2+的稳定性,进行如下实验,观察,记录结果.
实验Ⅰ(图1)
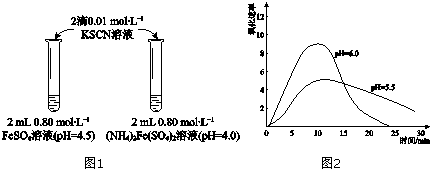
(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是NH4++H2O?NH3•H2O+H+(用化学用语表示).溶液的稳定性:
FeSO4<(NH4)2Fe(SO4)2(填“>”或“<”).
(2)甲同学提出实验Ⅰ中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+具有还原性.进行实验Ⅱ,否定了该观点,补全该实验.
(3)乙同学提出实验Ⅰ中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ:分别配制0.80mol•L-1 pH为1、2、3、4的FeSO4溶液,观察,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短.资料显示:亚铁盐溶液中存在反应 4Fe2++O2+10H2O?4Fe(OH)3+8H+.由实验Ⅲ,乙同学可得出的结论是溶液pH越小,Fe2+越稳定,原因是溶液中存在平衡4Fe2++O2+10H2O?4Fe(OH)3+8H+,c(H+)大,对平衡的抑制作用强,Fe2+更稳定.
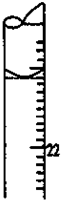
(4)进一步研究在水溶液中Fe2+的氧化机理.测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图2(实验过程中溶液温度几乎无变化).反应初期,氧化速率都逐渐增大的原因可能是生成的Fe(OH)3对反应有催化作用.
(5)综合以上实验,增强Fe2+稳定性的措施有加一定量的酸,密封保存.
实验Ⅰ(图1)

| 物质 | 0min | 1min | 1h | 5h |
| FeSO4 | 淡黄色 | 桔红色 | 红色 | 深红色 |
| (NH4)2Fe(SO4)2 | 几乎无色 | 淡黄色 | 黄色 | 桔红色 |
FeSO4<(NH4)2Fe(SO4)2(填“>”或“<”).
(2)甲同学提出实验Ⅰ中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+具有还原性.进行实验Ⅱ,否定了该观点,补全该实验.
| 操作 | 现象 |
| 取取2mLpH=4.0的0.80mol•L-1FeSO4溶液,加加2滴0.01mol•L-1KSCN溶液,观察. | 与实验Ⅰ中(NH4)2Fe(SO4)2溶液现象相同. |
(4)进一步研究在水溶液中Fe2+的氧化机理.测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图2(实验过程中溶液温度几乎无变化).反应初期,氧化速率都逐渐增大的原因可能是生成的Fe(OH)3对反应有催化作用.
(5)综合以上实验,增强Fe2+稳定性的措施有加一定量的酸,密封保存.
 某学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
某学生用0.1000mol•L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步: (1)根据无机含氧酸的酸性规律,将下列四种无机含氧酸按酸性相近两两组成一组,它们是①和④;②和③.(用序号表示)
(1)根据无机含氧酸的酸性规律,将下列四种无机含氧酸按酸性相近两两组成一组,它们是①和④;②和③.(用序号表示)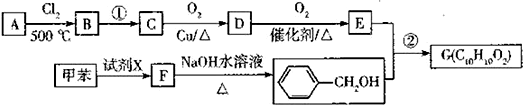
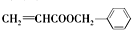 .
.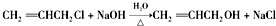 .
.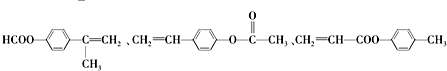 .
. .
.