题目内容
3.常温下,有无色溶液甲、乙、丙、丁四种,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和氨水溶液中的一种.已知甲、乙中水的电离程度均比纯水的小,甲、丙溶液的pH值大于7.则:甲是氨水 溶液,乙是盐酸溶液,丙是CH3COONa溶液;丁是NH4Cl溶液.分析 CH3COONa为强碱弱酸盐、NH4Cl为强酸弱碱盐,因水解可促进水的电离,四种溶液中CH3COONa溶液、氨水溶液呈碱性,pH大于7,以此解答该题.
解答 解:CH3COONa为强碱弱酸盐、NH4Cl为强酸弱碱盐,因水解可促进水的电离,盐酸和氨水抑制水的电离,甲、乙中水的电离程度均比纯水的小,应为盐酸和氨水中的物质,四种溶液中CH3COONa溶液、氨水溶液呈碱性,pH大于7,应为甲、丙,由此可知甲为氨水,则乙为盐酸,丙为CH3COONa,丁为NH4Cl,
故答案为:氨水;盐酸;CH3COONa;NH4Cl.
点评 本题考查无机物的推断,侧重于盐类水解的考查,注意把握盐类水解的规律和溶液酸碱性的判断,为解答该题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列广告用语在科学性上错误的是( )
| A. | 没有水就没有生命 | |
| B. | 这种蒸馏水绝对纯净,其中不含任何离子 | |
| C. | 这种口服液含丰富的氮、磷、锌等微量元素 | |
| D. | 这种饮料不含任何化学物质 |
11.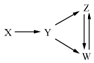 一定条件下,下列各组物质能一步实现如图所示转化关系的是( )
一定条件下,下列各组物质能一步实现如图所示转化关系的是( )
 一定条件下,下列各组物质能一步实现如图所示转化关系的是( )
一定条件下,下列各组物质能一步实现如图所示转化关系的是( )| 选项 | X | Y | Z | W |
| A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| B | Fe2O3 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | NH3 | N2 | NO | NO2 |
| A. | A | B. | B | C. | C | D. | D |
18.下列说法错误的是( )
| A. | 58.5g NaCl溶于1L水中配得1mol/L NaCl溶液 | |
| B. | 在标准状况下,44.8LHCl气体溶于水配成1L溶液,所得溶液中溶质的物质的量浓度为2mol/L | |
| C. | 在标准状况下,22.4L氨气溶于水配成1L溶液,从所得溶液中取出10mL,其物质的量浓度为1mol/L | |
| D. | 1mol/L的CaCl2溶液1L,取出100mL,含0.2molCl- |
8.工业上常用煤和水作原料经过多步反应制得氢气,其中一步的反应原理为:
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g)下面选项的条件中可判断该反应达到平衡状态的是( )
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g)下面选项的条件中可判断该反应达到平衡状态的是( )
| A. | 单位对间内消耗2mol的CO同时生成2mol的CO2 | |
| B. | 两个H-O键断裂的同时有一个H-H键断裂 | |
| C. | 反应容器内的压强不再发生变化 | |
| D. | 混合气体的相对分子质量不发生变化 |
15. 研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:
研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:
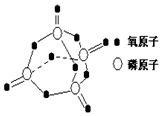
已知白磷的燃烧热为2378.0kJ/mol,白磷完全燃烧的产物结构如图所示,则表中X=433.75kJ•mol-1.
 研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:
研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
12.在碱性溶液中能大量共存且为无色透明的溶液是( )
| A. | K+、Cl-、MnO4-、SO42- | B. | Na+、K+、NO3-、CO32- | ||
| C. | Na+、NO3-、SO42-、HCO3- | D. | Na+、SO42-、H+、Cl- |