题目内容
12.下列叙述中正确的是( )| A. | 氯化铝溶液中加入过量氨水反应的实质是Al3++3NH3•H2O═Al(OH)3↓+3NH4 | |
| B. | 存在于污水中的细菌,常用投加明矾等电解质的方法进行处理 | |
| C. | 镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液 | |
| D. | 依据铝热反应原理,能发生反应2Al+3MgO═3Mg+Al2O3 |
分析 A.氯化铝溶液中加入过量氨水,反应生成氢氧化铝和氯化铵;
B.明矾溶液中的铝离子水解可以得到具有吸附性的氢氧化铝胶体,可以吸附悬浮杂质;
C.铝既可完全溶于过量盐酸又可完全溶于过量NaOH溶液,但是金属镁只和酸反应;
D.活泼金属能置换不活泼金属,铝热反应为铝置换出比铝不活泼的金属.
解答 解:A.氯化铝溶液中加入过量氨水反应生成氢氧化铝和氯化铵,离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故A正确;
B.明矾溶液中的铝离子水解可以得到具有净水作用的氢氧化铝胶体,可吸附悬浮物,但是不会处理污水中的重金属离子,故B错误;
C.镁和盐酸反应但不和氢氧化钠溶液反应,铝既和盐酸反应又和氢氧化钠溶液反应,所以镁铝合金不能完全溶于氢氧化钠溶液,故C错误;
D.镁的活泼性大于铝,所以铝不能置换镁,且活泼金属采用电解的方法冶炼,故D错误;
故选A.
点评 本题涉及离子共存、金属的冶炼、金属的性质等知识点,难度不大,注意氢氧化铝易溶于强碱但不溶于弱碱,为易错点.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
20.化学 与生产、生活息息相关,下列叙述错误的是( )
| A. | 光催化还原水制氢比电解水制氢更节能环保、更经济 | |
| B. | 铁表面镀锌可增强其抗腐蚀性 | |
| C. | 用聚乙烯塑料代替聚乳酸塑料可减少白色污染 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
17.分子式为C6H10O4,且能与NaHCO3反应的只含一种官能团的有机物共有(不含立体异构)( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
2.有Al、CuO、Fe2O3组成的混合物共10.0g,放入500mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250mL 2.0mol/L的NaOH溶液时,得到的沉淀最多.上述盐酸溶液的浓度为( )
| A. | 1mol/L | B. | 2 mol/L | C. | 0.5 mol/L | D. | 1.5 mol/L |

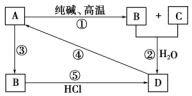 已知A是一种装饰品的主要成分,根据如图转化关系,回答下列问题.
已知A是一种装饰品的主要成分,根据如图转化关系,回答下列问题.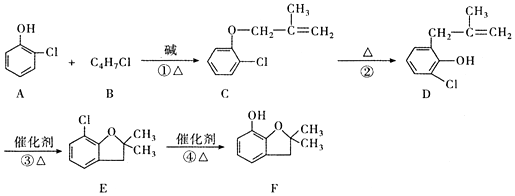
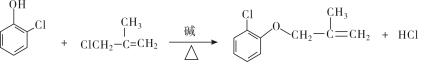 (有机物用结构简式表示,下同).
(有机物用结构简式表示,下同).