题目内容
1.0.1mol某烃在足量O2中完全燃烧,得到标准状况下13.44L CO2和5.4g水,该烃的分子式为( )| A. | CH4 | B. | C2H4 | C. | C3H8 | D. | C6H6 |
分析 根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$计算二氧化碳、水的物质的量,可确定有机物分子式,以此解答该题.
解答 解:n(CO2)=$\frac{13.44L}{22.4L/mol}$=0.6mol,n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,则0.1mol有机物含有0.6molC,0.6molH,则分子式为C6H6,
故选D.
点评 本题考查烃燃烧有关计算、有机物分子式确定,为高频考点,侧重于考查的分析、计算能力的考查,难度不大,注意掌握有机物燃烧有关规律.

练习册系列答案
相关题目
9.将2mol A气体和1mol B气体在固定体积的密闭容器中混合并在一定条件下发生如下反应并达到平衡状态:2A(g)+B(g)?2C(g),此反应为放热反应.下列能增大正、逆反应速率的方法是:
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
| A. | (1)(3)(5) | B. | (1)(3)(4) | C. | (1)(2)(4)(5) | D. | (1)(2)(3)(4)(5) |
1.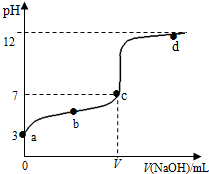 在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
(1)实验中的指示剂最好使用酚酞;
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡体系是A-+H2O?HA+OH-、H2O?H++OH-;
溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是c>b>a>d.
(4)该温度下,滴定曲线上c点时HA的电离平衡常数Ka=$\frac{1{0}^{-7}V}{20-V}$.(用含V的代数简式表示)
 在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:| V(NaOH)mL | 0.00 | 10.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
| pH | 3.0 | 4.7 | 5.7 | 6.7 | 7.7 | 8.7 | 9.7 | 10.7 | 11.7 | 12.5 |
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡体系是A-+H2O?HA+OH-、H2O?H++OH-;
溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是c>b>a>d.
(4)该温度下,滴定曲线上c点时HA的电离平衡常数Ka=$\frac{1{0}^{-7}V}{20-V}$.(用含V的代数简式表示)
8.下列对于NH3和CO2的说法中正确的是( )
| A. | 都是直线形结构 | |
| B. | 中心原子都采取sp1杂化 | |
| C. | NH3为三角锥形结构,CO2为直线形结构 | |
| D. | 氮原子和碳原子上都没有孤对电子 |
5.下列两种物质不属于同分异构体的是( )
| A. | 葡萄糖和果糖 | B. | 蔗糖和麦芽糖 | C. | 淀粉和纤维素 | D. | 正丁烷和异丁烷 |
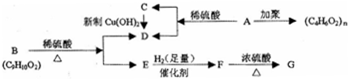
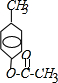 ;
;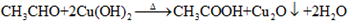 ,反应类型氧化反应;F→G
,反应类型氧化反应;F→G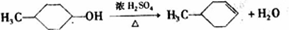 ,反应类型消去反应.
,反应类型消去反应.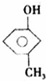 、
、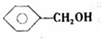 .
.