题目内容
1.(1)写出下面有机化合物的结构简式和键线式: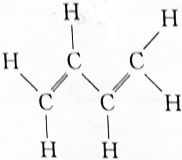 CH2=CH-CH=CH2、=-=.
CH2=CH-CH=CH2、=-=.(2)某有机物的键线式结构为
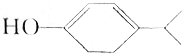 ,则它的分子式为C9H14O,其官能团为羟基和碳碳双键,它属于脂环化合物(填“芳香化合物”或“脂环化合物”)
,则它的分子式为C9H14O,其官能团为羟基和碳碳双键,它属于脂环化合物(填“芳香化合物”或“脂环化合物”)
分析 结构简式是指把分子中各原子连接方式表示出来的式子,通常只适用于以分子形式存在的纯净物.应表现该物质中的官能团:只要把碳氢单键省略掉即可,碳碳单键、碳氯单键、碳和羟基的单键等大多数单键可以省略也可不省略;
键线式中用短线“-”表示化学键,端点、交点表示碳原子,C原子、H原子不需要标出;
据此解答.
解答 解:(1) 的结构简式为CH2=CH-CH=CH2,碳碳双键为官能团不能省略;键线式为:=-=;
的结构简式为CH2=CH-CH=CH2,碳碳双键为官能团不能省略;键线式为:=-=;
故答案为:CH2=CH-CH=CH2;=-=;
(2) 中含有9个C,14个H,1个O,分子式为:C9H14O;官能团为羟基和碳碳双键;含有环,但是不是苯环,所以属于脂环化合物;
中含有9个C,14个H,1个O,分子式为:C9H14O;官能团为羟基和碳碳双键;含有环,但是不是苯环,所以属于脂环化合物;
故答案为:C9H14O;羟基和碳碳双键;脂环化合物;
点评 本题考查了有机化合物表示方法及分类,明确有机化合物结构简式、键线式书写方法是解题关键,题目难度不大.

练习册系列答案
相关题目
13.1molRO4-能氧化5mol的Fe2+,则在还原产物中R元素的化合价( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
10.X、Y、Z、W是原子序数依次增大的4种短周期元素.X与Z位于同一主族,X原子的最外层电子数是次外层电子数的2倍,Y元素的单质既能与盐酸反应又能与NaOH溶液反应,X、Y、Z、W原子的最外层电子数之和为18.下列说法不正确的是( )
| A. | X单质在一定条件下能与Z的最高价氧化物发生置换反应 | |
| B. | 原子半径:Y>Z>W | |
| C. | 最高价氧化物对应水化物的酸性由弱到强的顺序:X<Z<W | |
| D. | 室温下,0.1mol/LW的气态氢化物的水溶液的pH=1 |
17.下表是部分短周期元素在周期表中的相对位置关系,试完成以下题目:
(1)表中元素⑤的氯化物的化学式为NCl3,此氯化物的水溶液显酸性.
(2)写出元素⑦在周期表中的位置为第三周期第ⅡA族.
(3)写出元素⑧的单质与NaOH溶液反应的化学方程式2Al+2H2O+2NaOH═2NaAlO2+3H2↑.
(4)某元素的单质在与大气的平流层中能吸收紫外线,被称为地球生物的“保护伞”,则该元素在表中的序号为⑤,该元素的名称为臭氧
(5)元素⑩的单质是一种污染大气的气体,试写出在实验室中吸收该气体的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
| 族 短周期 | ⅠA | ||||||
| ① | |||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||
| ⑦ | ⑧ | ⑨ | ⑩ |
(2)写出元素⑦在周期表中的位置为第三周期第ⅡA族.
(3)写出元素⑧的单质与NaOH溶液反应的化学方程式2Al+2H2O+2NaOH═2NaAlO2+3H2↑.
(4)某元素的单质在与大气的平流层中能吸收紫外线,被称为地球生物的“保护伞”,则该元素在表中的序号为⑤,该元素的名称为臭氧
(5)元素⑩的单质是一种污染大气的气体,试写出在实验室中吸收该气体的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
6.下列有机化合物中,可以看作醇类的是( )
| A. | 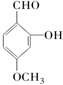 | B. |  | ||
| C. | 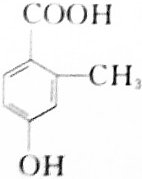 | D. | 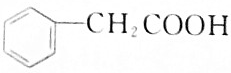 |
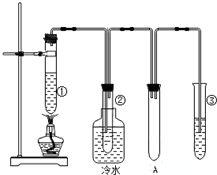 石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已忽略).在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水.
石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已忽略).在试管①中加入石蜡油和氧化铝(催化石蜡分解);试管②放在冷水中,试管③中加入溴水.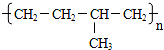 B.
B.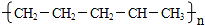
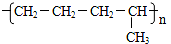 D.
D.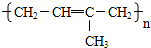
 A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )
A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )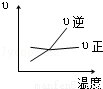 B.
B.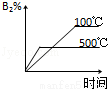 C.
C.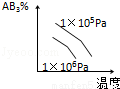 D.
D.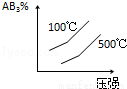
 O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)
O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)