题目内容
在无色透明的溶液中可以大量共存的离子组是( )
| A、H+、K+、Fe2+、NO3- |
| B、OH-、Cl-、Na+、NH4+ |
| C、Cu2+、NO3-、OH-、Cl- |
| D、Mg2+、K+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:无色溶液说明不含有颜色的离子,离子之间不反应生成气体、沉淀、弱电解质、络合物或发生氧化还原反应、双水解反应的就能共存,据此分析解答.
解答:
解:A.酸性条件下Fe2+、NO3-发生氧化还原反应生成铁离子、NO且亚铁离子呈浅绿色,所以不符合题意,故A错误;
B.OH-、NH4+反应生成弱电解质一水合氨,所以不能大量共存,故B错误;
C.Cu2+、OH-生成氢氧化铜沉淀且 铜离子呈蓝色,所以不符合条件,故C错误;
D.这几种离子之间不反应且都是无色的,符合条件,故D正确;
故选D.
B.OH-、NH4+反应生成弱电解质一水合氨,所以不能大量共存,故B错误;
C.Cu2+、OH-生成氢氧化铜沉淀且 铜离子呈蓝色,所以不符合条件,故C错误;
D.这几种离子之间不反应且都是无色的,符合条件,故D正确;
故选D.
点评:本题考查离子共存,为高考高频点,明确离子性质及离子共存条件是解本题关键,注意题干中限制性条件,有时还常常与pH、盐类水解、氧化还原反应等联合考查,易错选项是A,题目难度中等.

练习册系列答案
相关题目
S-诱抗素的分子结构如图所示,下列关于该物质的说法正确的是( )
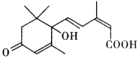

| A、其分子式为C15H22O4 |
| B、1 mol该物质与足量NaOH溶液反应,最多消耗2 mol NaOH |
| C、一定条件下,l mol该有机物最多可与4 mol氢气发生加成反应 |
| D、既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
常温下,下列溶液中能大量共存的离子是( )
A、在
| ||
| B、由水电离出的c(H+)和c(OH-)浓度的乘积为10-22的溶液H+、K+、ClO-、SO42- | ||
| C、在pH=7的溶液中,Fe3+、K+、Cl-、SO32- | ||
| D、甲基橙显红色的溶液中,Na+、K+、Cl-、S2O32- |
下列各组离子在指定溶液中一定能大量共存的是( )
| A、无色溶液中:K+、Cu2+、Na+、SO42- |
| B、强酸性溶液中:Al3+、NO3-、I-、Cl- |
| C、pH=11的溶液中:Na+、CO32-、AlO2-、NO3- |
| D、加入Al能放出H2的溶液中:NH4+、Cl-、HCO3-、NO3- |
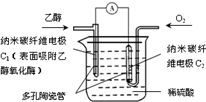 生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应方程式为:C2H5OH+3H2O-12e-=2CO2+12H+.下列说法不正确的是( )
生物燃料电池(BFC)是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示.已知C1极的电极反应方程式为:C2H5OH+3H2O-12e-=2CO2+12H+.下列说法不正确的是( )| A、C1极为电池负极,C2极为电池正极 |
| B、C2极的电极反应式为O2+4H++4e-=2H2O |
| C、该生物燃料电池的总反应方程式为C2H5OH+3O2=2CO2+3H2O |
| D、电子由C2极经外电路导线流向C1极 |
下列排列顺序正确的是( )
| A、常温下水电离出的c(H+):pH=5的CH3COOH溶液>pH=5的盐酸 |
| B、微粒半径:Fe(OH)3胶粒>K+>C1->Na+ |
| C、等温等物质的量浓度溶液的pH:Na2CO3>苯酚钠>NaHCO3 |
| D、氢化物的沸点:H2Se>H2S>H2O |