题目内容
有一白色固体混合物,可能含有的阴、阳离子分别是
为了鉴定其中的离子,现进行如下实验,根据实验现象,填写下列表格:
(1)取该粉末,加水后得到无色溶液;用pH试纸测得溶液的pH为12.据此可排除 离子,排除的原因
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出.据此,可肯定含有 离子;同时可排除 离子.
(3)根据(1)和(2)的结论,固体中还有未确定的阳离子有 ,检验的方法和现象是 .
| 阳离子 | Ba2+ Ag+ Mg2+ Na+ |
| 阴离子 | SO42- SO32- CO32- AlO2- |
(1)取该粉末,加水后得到无色溶液;用pH试纸测得溶液的pH为12.据此可排除
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出.据此,可肯定含有
(3)根据(1)和(2)的结论,固体中还有未确定的阳离子有
考点:物质的检验和鉴别的实验方案设计,常见离子的检验方法
专题:离子反应专题
分析:(1)取该粉末,加水后得到无色溶液;用pH试纸测得溶液的pH为12,则溶液显碱性,不能存在Ag+、Mg2+;
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,说明含有AlO2-,同时有无色无味气体逸出,结合阴离子分析只有碳酸根离子符合,碳酸根离子和钡离子结合生成白色沉淀,亚硫酸根离子和盐酸反应生成无色有刺激性气味的气体二氧化硫,则一定不含有Ba2+、SO32-;
(3)由上述分析可知阳离子Na+不能确定,利用焰色反应进行验证.
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,说明含有AlO2-,同时有无色无味气体逸出,结合阴离子分析只有碳酸根离子符合,碳酸根离子和钡离子结合生成白色沉淀,亚硫酸根离子和盐酸反应生成无色有刺激性气味的气体二氧化硫,则一定不含有Ba2+、SO32-;
(3)由上述分析可知阳离子Na+不能确定,利用焰色反应进行验证.
解答:
解:(1)取该粉末,加水后得到无色溶液;用pH试纸测得溶液的pH为12,则溶液显碱性,离子之间不能结合生成沉淀,则不能存在Ag+、Mg2+,
故答案为:Ag+、Mg2+;碱性溶液中Ag+、Mg2+转化为沉淀;
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,沉淀为氢氧化铝,则说明原溶液中含有AlO2-,同时有无色无味气体逸出,气体只能为二氧化碳,只有碳酸根离子符合,碳酸根离子和钡离子结合生成白色沉淀,亚硫酸根离子和盐酸反应生成无色有刺激性气味的气体二氧化硫,则一定不含有Ba2+、SO32-,
故答案为:AlO2-;Ba2+、SO32-;
(3)由上述分析可知阳离子Na+不能确定,利用焰色反应进行验证,利用焰色反应,用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧出现黄色火焰,说明一定含有钠离子,
故答案为:Na+;利用焰色反应,用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧出现黄色火焰,说明一定含有钠离子.
故答案为:Ag+、Mg2+;碱性溶液中Ag+、Mg2+转化为沉淀;
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,沉淀为氢氧化铝,则说明原溶液中含有AlO2-,同时有无色无味气体逸出,气体只能为二氧化碳,只有碳酸根离子符合,碳酸根离子和钡离子结合生成白色沉淀,亚硫酸根离子和盐酸反应生成无色有刺激性气味的气体二氧化硫,则一定不含有Ba2+、SO32-,
故答案为:AlO2-;Ba2+、SO32-;
(3)由上述分析可知阳离子Na+不能确定,利用焰色反应进行验证,利用焰色反应,用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧出现黄色火焰,说明一定含有钠离子,
故答案为:Na+;利用焰色反应,用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧出现黄色火焰,说明一定含有钠离子.
点评:本题考查物质的检验和鉴别,为高频考点,把握常见离子的性质及检验方法为解答的关键,侧重分析与推断能力的综合考查,题目难度不大.

练习册系列答案
相关题目
下列关于钠及其化合物的说法正确的是( )
| A、钠的化学活泼性很强,钠着火必须及时用泡沫灭火器扑灭 |
| B、氧化钠和过氧化钠都是白色固体,都是碱性氧化物 |
| C、将金属钠投入水中,生成氢氧化钠,同时放出O2 |
| D、少量钠通常保存在煤油里 |
硬水和软水的本质区别是( )
| A、硬水浑浊、软水澄清 |
| B、硬水含有杂质、软水含杂质少 |
| C、硬水含有较多可溶性钙镁化合物、软水不含或含少量可溶性钙镁化合物 |
| D、硬水是不纯净水,软水是纯净水 |
H2A为二元弱酸在0.1mol?L-1Na2A溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A2-)>c(H+)>c(HA-)>c(OH-) |
| B、2 c(Na+)=c(A2-)+c(HA-)+c(H2A) |
| C、c(OH-)=c(H+)+c(HA-)+c(H2A) |
| D、c(Na+)+c(H+)=2 c(A2-)+c(OH-)+c(HA-) |
V mL Al2(SO4)3溶液中含Al3+a g,取
mL溶液稀释到4V mL,则稀释后溶液中SO42-的物质的量浓度是( )
| V |
| 4 |
A、
| ||
B、
| ||
C、
| ||
D、
|
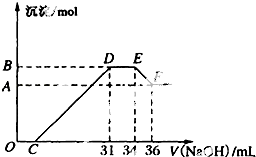 某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐.在反应后的溶液中,逐滴加入4mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示.分析图象回答问题:
某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐.在反应后的溶液中,逐滴加入4mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示.分析图象回答问题:
 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)△H=a kJ?mol-1,测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)△H=a kJ?mol-1,测得CO2和CO浓度随时间的变化如图所示: