题目内容
(12分)铁钾矾[KxFey(SO4)m·nH2O]常用作工业媒染剂。其组成可用如下方法测定:
①准确称取2.0120g样品配成100mL溶液A。
②准确量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.466g。
③准确量取25.00mL溶液A,加入足量的KI溶液,以淀粉为指示剂,用0.1250 mol·L-1的Na2S2O3溶液滴定,消耗8.00mL至终点(已知:I2+2Na2S2O3=2NaI+Na2S4O6)。
(1)要检验出A溶液中存在的Fe3+,可以加入 溶液。
(2)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1.0×10-5 mol?L-1,应保持溶液中c(Ba2+)≥ mol·L-1。
(3)步骤③中判断滴定终点的方法是 。
(4)通过计算确定铁钾矾的组成(写出计算过程)。
(1)KSCN(或硫氰化钾)(2分) (2)1.1×10-5 (2分)
(3)滴入最后一滴Na2S2O3溶液时,锥形瓶中溶液蓝色褪去,且半分钟内不恢复(2分)
(4)25.00mLA溶液中:
n(SO42-)=0.4660g/233g? mol -1=2×10-3mol
n(Fe3+)=0.1250mol?L-1×8.0×10-3L=1×10-3mol (2分)
根据电荷守恒:n(K+)=2×2×10-3mol-3×1×10-3mol=1×10-3mol
根据质量守恒,结晶水的物质的量:
[2.0120g×(25/100)-1×10-3mol×(39+56)mol?L-1-2×10-3mol×96g?mol-1]/18g?mol-1
=1.2×10-2mol (2分)
所以x∶y∶m∶n=1∶1∶2∶12,化学式为:KFe(SO4)2?12H2O
答:样品的组成为KFe(SO4)2?12H2O。 (2分)
【解析】
试题分析:(1)铁离子能与KSCN溶液反应使溶液显红色,所以要检验出A溶液中存在的Fe3+,可以加入KSCN(或硫氰化钾)溶液。
(2)已知室温下BaSO4的Ksp=1.1×10-10,欲使溶液中c(SO42-)≤1.0×10-5 mol?L-1,则应保持溶液中c(Ba2+)≥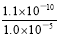 =1.1×10-5mol·L-1。
=1.1×10-5mol·L-1。
(3)由于碘遇淀粉显蓝色,所以步骤③中判断滴定终点的方法是滴入最后一滴Na2S2O3溶液时,锥形瓶中溶液蓝色褪去,且半分钟内不恢复。
(4)25.00mLA溶液中:n(SO42-)=0.4660g/233g? mol -1=2×10-3mol
n(Fe3+)=0.1250mol?L-1×8.0×10-3L=1×10-3mol
根据电荷守恒可知:n(K+)=2×2×10-3mol-3×1×10-3mol=1×10-3mol
根据质量守恒可知结晶水的物质的量=[2.0120g×(25/100)-1×10-3mol×(39+56)mol/L-2×10-3mol×96g/mol]/18g?mol-1=1.2×10-2mol
所以x∶y∶m∶n=1∶1∶2∶12
即化学式为KFe(SO4)2?12H2O
考点:考查铁离子检验、滴定实验、溶度积常数应用以及物质化学式测定等

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案