题目内容
(1)3 mol二氧化碳气体中,约含有 个二氧化碳分子;2molNH4+中共有 mol电子,与之电子数相等的H2O的质量是 ,这些水若完全电解,产生的氢气在标准状况下的体积为 L。
(2)相同质量的氧气、氢气、二氧化碳中,含有分子数目最少的是 (填化学式,下同),标准状况下体积最大的是 ,原子数最少的是 。
(3)在NaCl与MgCl2的混合液中,Na+与Mg2+的物质的量之比为1:2。如果混合液中共有0.5 mol Cl-,溶液的体积为0.5 L,则混合液中氯化钠的质量为 ;MgCl2的物质的量浓度为 。
练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
20.能正确表示下列反应的离子方程式的是( )
| A. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| B. | 氯化钠与浓硫酸混合加热:H++Cl-$\frac{\underline{\;\;△\;\;}}{\;}$HCl↑ | |
| C. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| D. | 明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓ |
1.下列物质属于电解质的是( )
| A. | 铁 | B. | 二氧化碳 | C. | 浓硫酸 | D. | 氯化钙 |
18.化学与生活、生产、环境密切相关. 下列说法不正确的是( )
| A. | 工厂排放 CO2会导致酸雨的形成 | |
| B. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 | |
| C. | “山东疫苗案”涉及疫苗未冷藏储运而失效,这与蛋白质变性有关 | |
| D. | 《黄白第十六》中有“曾青涂铁,铁赤如铜”,这与化学变化有关 |
5.下列有关实验操作正确的是( )
| 实验 | 操作 | |
| A | 配制0.1mol•L-1氯化铝溶液 | 先将氯化铝晶体溶于浓盐酸中,后加蒸馏水稀释至指定体积 |
| B | 在加热条先下氢气还原氧化铜 | 反应完成后,先停止通入氢气,后停止加热 |
| C | 浓盐酸与碳酸钙反应制备CO2 | 气体产物先通过浓硫酸,后通过饱和碳酸氢钠溶液 |
| D | 检验某溶液是否含SO42- | 先加入BaCl2溶液,后加入盐酸 |
| A. | A | B. | B | C. | C | D. | D |
6.已知2A2(g)+B2(g)?2C3(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA2和1molB2,在500℃时充分反应达平衡后C3的浓度为wmol/L,放出热量bkJ.
(1)比较a>b(填>、=、<)
(2)下表为不同温度下该反应的平衡常数.
若在原来的容器中,只加入2molC3,500℃时充分反应达平衡后,吸收热量ckJ,C3的浓度=(填>、=、<)wmol/L,a、b、c之间满足何种关系a=b+c(用代数式表示).
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA2和1molB2,500℃时充分反应达平衡后,放出热量dkJ,则d>b(填>、=、<).
(5)在一定温度下,向一个容积不变的容器中,通入3molA2 和2molB2及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为4molA2、3molB2、2molC3,则平衡时A2的转化率变大(填“不变”、“变大”、“变小”或“不能确定”)
(6)碳酸锶广泛应用于电子工业.以天青石(主要成分为SrSO4)为基本原料制备碳酸锶.(已知:Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.1×10-10.)
①将天青石矿粉与Na2CO3溶液搅拌混匀、加热,发生的离子反应方程式为:SrSO4+CO32-═SrCO3+SO42-.
②当转化完成时,混合液中c(CO32-)=1.0×10-3mol/L,c(SO42-)=2.91mol/L.
(1)比较a>b(填>、=、<)
(2)下表为不同温度下该反应的平衡常数.
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA2和1molB2,500℃时充分反应达平衡后,放出热量dkJ,则d>b(填>、=、<).
(5)在一定温度下,向一个容积不变的容器中,通入3molA2 和2molB2及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为4molA2、3molB2、2molC3,则平衡时A2的转化率变大(填“不变”、“变大”、“变小”或“不能确定”)
(6)碳酸锶广泛应用于电子工业.以天青石(主要成分为SrSO4)为基本原料制备碳酸锶.(已知:Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.1×10-10.)
①将天青石矿粉与Na2CO3溶液搅拌混匀、加热,发生的离子反应方程式为:SrSO4+CO32-═SrCO3+SO42-.
②当转化完成时,混合液中c(CO32-)=1.0×10-3mol/L,c(SO42-)=2.91mol/L.
3.下列实验操作及现象与实验结论一致的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液,生成白色沉淀 | 该溶液中不一定含有SO42- |
| B | 光洁的铁钉放在冷的浓硫酸中,无明显现象 | 铁钉与冷的浓硫酸不反应 |
| C | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡静置,下层分别呈无色和紫红色 | 氧化性:Br2>Fe3+>I2 |
| D | 向浓度均为0.1mol•L-1的KCl、KI混合溶液中滴加1~2滴0.01mol•L-1的AgNO3溶液,产生的沉淀呈黄色 | Ksp(AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |



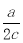 L C.ac L D.2ac L
L C.ac L D.2ac L