题目内容
设NA为阿伏加德罗常数,下列叙述中,正确的是( )
| A、标准状况下,NH3和CH4的混合气体2.24L,所含电子总数为2NA |
| B、7g CnH2n中含氢原子数为NA |
| C、78 g 过氧化钠与CO2反应,转移电子数为2NA |
| D、25℃时,0.1mol/L的NaOH溶液中,含有钠离子数为0.1NA |
考点:阿伏加德罗常数
专题:
分析:A、2.24L NH3和CH4的混合气体,标准状况下都是0.1mol,总共含有1mol电子.
B、最简式是CH2,7gCnH2n中含有0.5molCH2,含有1mol氢原子;
C、过氧化钠与二氧化碳的反应中,过氧化钠既是氧化剂也是氧化剂,过氧化钠中氧元素为-1价,根据生成氧气的物质的量计算出转移的电子数;
D、溶液体积不明确.
B、最简式是CH2,7gCnH2n中含有0.5molCH2,含有1mol氢原子;
C、过氧化钠与二氧化碳的反应中,过氧化钠既是氧化剂也是氧化剂,过氧化钠中氧元素为-1价,根据生成氧气的物质的量计算出转移的电子数;
D、溶液体积不明确.
解答:
解:A、标准状况下,2.24L NH3和CH4的混合气体的物质的量是0.1mol,含有1mol电子,所含电子总数为NA,故A错误;
B、7gCnH2n中含0.5mol最简式CH2,含有的氢原子的物质的量是1mol,氢原子数为NA,故B正确;
C、78g过氧化钠的物质的量为1mol,1mol过氧化钠与足量二氧化碳反应生成0.5mol氧气,转移了1mol电子,转移电子数为NA,故C错误;
D、溶液体积不明确,无法计算溶液中钠离子的个数,故D错误.
故选B.
B、7gCnH2n中含0.5mol最简式CH2,含有的氢原子的物质的量是1mol,氢原子数为NA,故B正确;
C、78g过氧化钠的物质的量为1mol,1mol过氧化钠与足量二氧化碳反应生成0.5mol氧气,转移了1mol电子,转移电子数为NA,故C错误;
D、溶液体积不明确,无法计算溶液中钠离子的个数,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在一定温度下,在一个密闭容器中加入H2和I2蒸气各0.5mol,发生反应H2+I2?2HI,达到平衡时,生成HI 0.8mol,若其它条件不变,开始充入的H2为2mol,则达到平衡时生成的HI可能是下列中的( )
| A、1.1 mol |
| B、0.87 mol |
| C、0.8 mol |
| D、0.5 mol |
下列物质的水溶液能够导电,但属于非电解质的是( )
| A、四氯化碳 | B、二氧化硫 |
| C、氯化氢 | D、氯气 |
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法或表示式正确的是( )
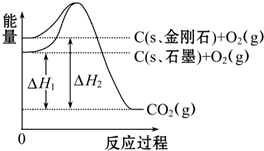

| A、C(s、石墨)═C(s、金刚石)△H=+1.9 kJ?mol-1 |
| B、石墨和金刚石的转化是物理变化 |
| C、金刚石的稳定性强于石墨 |
| D、1 mol石墨的能量比1 mol金刚石的总能量大 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0,在恒容的密闭容器中,下列有关说法正确的是( )
| 130℃ |
| 催化剂 |
| A、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B、平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C、单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
| D、其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
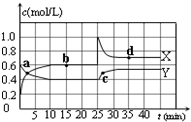 已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
已知:2NO2(g)?N2O4(g);△H<0.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示. 一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO): 某有机物M的球棍模型如图所示:
某有机物M的球棍模型如图所示: