题目内容
19.已知aAn-、bBm-、cCm+、dDn+四种离子具有相同的核外电子排布,且n>m,则下列关系中正确的是( )| A. | 得电子能力:A>B>Cm+>Dn+ | B. | 还原性:An->Bm->C>D | ||
| C. | 原子半径:D>C>B>A | D. | 离子半径:An->Bm->Cm+>Dn+ |
分析 aAn-、bBm-、cCm+、dDn+具有相同的电子层结构,a、b、c、d不相等且n>m,属于四种不同元素的离子,且a+n=b+m=c-m=d-n,故原子序数大小顺序是d>c>b>a,结合离子所得电荷可知,A、B为非金属元素,非金属性:B>A,C、D为金属元素,金属性:C>D,且C、D位于A和B的下一周期,电子层结构相同,核电荷数越大离子半径越小,据此分析.
解答 解:aAn-、bBm-、cCm+、dDn+具有相同的电子层结构,a、b、c、d不相等且n>m,属于四种不同元素的离子,且a+n=b+m=c-m=d-n,故原子序数大小顺序是d>c>b>a,结合离子所得电荷可知,A、B为非金属元素,非金属性:B>A,C、D为金属元素,金属性:C>D,且C、D位于A和B的下一周期.
A.同周期元素的原子序数越大,非金属性越强,得电子能力越强,则得电子能力:B>A,故A错误;
B.非金属性越强,阴离子的还原性越弱,金属性越强,还原性越强,一般金属的还原性大于非金属阴离子,则还原性:C>D>An->Bm-,故B错误;
C.电子层越多,原子半径越大,电子层相同,原子序数越大,半径越小,则原子半径:C>D>A>B,故C错误;
D.核电荷数a>b>d>c,电子层结构相同,核电荷数越大离子半径越小,故离子半径:An->Bm->Cm+>Dn+,故D正确,
故选D.
点评 本题考查原子结构与元素周期律,确定元素在周期表中的相对位置是关键,注意理解掌握微粒半径的比较规律,难度中等,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
9.影响化学反应速率的因素很多,某课外兴趣小组用实验的方法研究反应速率的有关问题.
(1)实验1 探究Mg与盐酸反应速率的变化规律
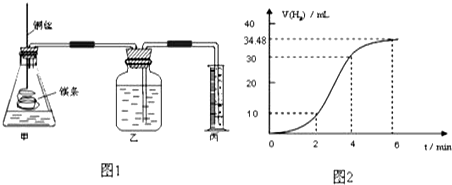
取一段镁条,用砂纸擦去表面的氧化膜,铜丝缠着镁条伸入装置甲中,使镁条浸入锥形瓶内的体积为2L稀盐酸(足量)中.镁条和盐酸反应生成H2的体积与反应时间的关系曲线如图2所示.
①从图2中看出0-6min内平均反应速率最快的时间段是B.(填代号)
A.0-2min B.2-4min C.4-6min
②请计算4-6min 时间内,用HCl表示的平均反应速率为1×10-4mol/(L•min).(假设图2氢气体积均已换算为标准状况下的体积,且溶液体积变化可忽略)
③图1装置甲中与镁条相连的铜丝若一起浸入稀盐酸中对反应速率影响下列说法正确的是(
A.加快反应速率但生成氢气的总量不变 B.减慢反应但增大生成氢气总量
C.不影响反应速率 D.加快反应速率但生成氢气的总量减小
(2)实验2 探究酸浓度对MnO2与H2O2反应速率的影响:已知MnO2+H2O2+2H+ Mn2++O2↑+2H2O,现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间.
①上表中V1=5.0mL,V3=1.5mL.
②有同学提出实验I不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是实验I中MnO2将作为催化剂,其他三组实验中二氧化锰作氧化剂,反应原理不同,且酸量不同.
③若实验测得t2>t3>t4,则可得出的实验结论是酸浓度越大,反应速率越快.
(1)实验1 探究Mg与盐酸反应速率的变化规律

取一段镁条,用砂纸擦去表面的氧化膜,铜丝缠着镁条伸入装置甲中,使镁条浸入锥形瓶内的体积为2L稀盐酸(足量)中.镁条和盐酸反应生成H2的体积与反应时间的关系曲线如图2所示.
①从图2中看出0-6min内平均反应速率最快的时间段是B.(填代号)
A.0-2min B.2-4min C.4-6min
②请计算4-6min 时间内,用HCl表示的平均反应速率为1×10-4mol/(L•min).(假设图2氢气体积均已换算为标准状况下的体积,且溶液体积变化可忽略)
③图1装置甲中与镁条相连的铜丝若一起浸入稀盐酸中对反应速率影响下列说法正确的是(
A.加快反应速率但生成氢气的总量不变 B.减慢反应但增大生成氢气总量
C.不影响反应速率 D.加快反应速率但生成氢气的总量减小
(2)实验2 探究酸浓度对MnO2与H2O2反应速率的影响:已知MnO2+H2O2+2H+ Mn2++O2↑+2H2O,现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间.
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
②有同学提出实验I不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是实验I中MnO2将作为催化剂,其他三组实验中二氧化锰作氧化剂,反应原理不同,且酸量不同.
③若实验测得t2>t3>t4,则可得出的实验结论是酸浓度越大,反应速率越快.
10.下列叙述中,与胶体性质无直接关系的是( )
| A. | 含有少量硫的酒精溶液,加入大量水后形成乳白色液体,用滤纸过滤不能分离出硫 | |
| B. | 原硅酸溶液中加入硫酸铵饱和溶液,结果产生沉淀 | |
| C. | 硫酸铜溶液中加入硫化钠溶液产生黑色沉淀 | |
| D. | 用水稀释牛奶,用一束强光照射,从侧面观察,可以看到一条清晰的光路 |
7.分离苯和苯酚的混合物,通常采用的方法是( )
| A. | 振荡混合物,用分液漏斗分离 | |
| B. | 加入NaOH溶液后振荡,用分液漏斗分离;取下层液体通入CO2,待分层后分液 | |
| C. | 加水振荡后用分液漏斗分离 | |
| D. | 加稀盐酸振荡后,用分液漏斗分离 |
4.下列物质的电子式正确的是( )
| A. | 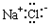 | B. | 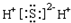 | C. |  | D. | 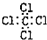 |
11.有四组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如表所示:
下列各项判断正确的是( )
| 第一组 | A-268.8 | B-249.5 | C-185.8 | D-151.7 |
| 第二组 | F2-187.0 | Cl2-33.6 | Br2 58.7 | I2 184.0 |
| 第三组 | HF 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | H2Se 42.0 | H2Te-1.8 |
| A. | 第一组和第二组物质中一定含有共价键 | |
| B. | 第三组与第四组相比较,化合物的稳定顺序为:HBr>H2Se | |
| C. | 第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI | |
| D. | 第四组物质中H2O的沸点最高,是因为H2O分子中化学键键能最强 |
8.为了研究外界条件对过氧化钠分解速率的影响,某同学做了以下实验.
(1)①中过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;三氯化铁\;}}{\;}$2H2O+O2↑.
(2)实验①的目的是研究温度对H2O2分解速率的影响.
(3)实验②的目的是探究温度和催化剂对反应速率的影响,为达到使用目的,还需进行的后续操作是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率.(所用试剂限本实验中提供的).
(4)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:如图所示.同学们分别从定性和定量角度进行了比较.
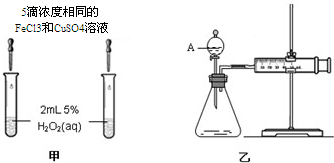
①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是:控制阴离子相同,排除阴离子的干扰.
②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是产生40ml气体所需要的时间.
| 编号 | 操 作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中. | 试管A中不再产生气泡;试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液. | 试管A、B中均未明显见到有气泡产生 |
(2)实验①的目的是研究温度对H2O2分解速率的影响.
(3)实验②的目的是探究温度和催化剂对反应速率的影响,为达到使用目的,还需进行的后续操作是将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率.(所用试剂限本实验中提供的).
(4)对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:如图所示.同学们分别从定性和定量角度进行了比较.

①定性分析:如图甲可通过观察溶液中气泡产生的速率,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是:控制阴离子相同,排除阴离子的干扰.
②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是产生40ml气体所需要的时间.
9.下列说法错误的是( )
| A. | ⅦA元素的氢化物中氟化氢的沸点最高 | |
| B. | 第三周期元素形成的简单离子的半径随原子序数的增大依次增大 | |
| C. | I2易溶于CCl4可以用相似相溶原理解释 | |
| D. | CH2=CH2分子中共有5个σ键和1个π键 |
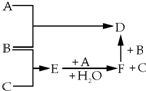 有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.
有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.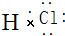 ;
;