题目内容
18.将足量的铜屑加入到浓度均为2mol/L的HNO3和H2SO4的混合溶液100ml中,充分反应后,求溶液中Cu2+浓度(假设溶液体积不变).分析 发生反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,铜足量,溶液中n(NO3-)=0.2mol,n(H+)=0.2mol+0.2mol×2=0.6mol,由反应可知,氢离子不足,根据氢离子计算参加反应Cu的物质的量,进而计算溶液中Cu2+浓度.
解答 解:混合溶液中n(NO3-)=0.1L×2mol/L=0.2mol,n(H+)=0.2mol+0.1L×2mol/L×2=0.6mol,
Cu足量,由3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,可知0.2molNO3-完全反应需要0.8molH+离子,大于溶液中0.6molH+离子,故H+离子不足,则参加反应Cu为0.6mol×$\frac{3}{8}$,溶液中Cu2+浓度$\frac{0.6×\frac{3}{8}}{0.1}$=2.25mol/L,
答:溶液中Cu2+浓度为:2.25mol/L.
点评 本题考查化学方程式有关计算,注意酸性条件下,硝酸根具有强氧化性,关键是明确反应本质,利用离子方程式解答,难度中等.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案
相关题目
8.下列说法正确的是( )
| A. | H2O(g)=H2O(l)△H=-44kJ/mol,所以该过程是放热反应 | |
| B. | 人类利用的能源都是通过化学反应获得的 | |
| C. | 2CO(g)+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2(g)△H<0,则56gCO和32gO2所具有的总能里大于88g所具有的总能量 | |
| D. | 需要加热的反应一定是吸热反应 |
6.将29.5g乙烷和乙烯的混合气体通入足量的溴水后,溴水质量增加7g,则混合气体中乙烯的体积分数是( )
| A. | 21% | B. | 25% | C. | 30% | D. | 35% |
13.某主族元素原子,其M能层上有一个半充满的能级,该原子的质子数( )
| A. | 只能是11 | B. | 只能是24 | C. | 可能是29 | D. | 可能是11或15 |
3.下列关于元素周期表的叙述,错误的是( )
| A. | 元素周期表揭示了化学元素间的内在联系,是化学发展史上重要里程碑 | |
| B. | 在周期表中,把电子层数相同的元素排成一横行,称为一周期 | |
| C. | 元素周期表中,总共有18个纵行,18个族,IIIB族含有32种金属元素 | |
| D. | 第IA族(除H)元素又称为碱金属元素,第ⅦA族元素又称为卤族元素 |
10.下列说法正确的是( )
| A. | KOH和CaCl2既含有离子键,又含有共价键 | |
| B. | PH3各原子均满足8电子稳定结构 | |
| C. | 硫离子的结构示意图: | |
| D. | NH4Cl的电子式: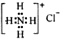 |
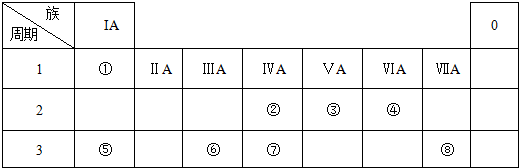
7.下表为元素周期表的一部分,请回答有关问题:
(1)⑤和⑧的元素符号是Si和Ar;
(2)表中最活泼的金属元素是K,非金属性最强的元素是F(用元素符号填写);
(3)写出⑦和⑨形成的化合物的电子式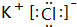
(4)①的氢化物与⑦的氢化物能够发生反应,写成形成盐M的电子式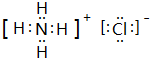 ,M中的化学键类型为离子键、共价键.
,M中的化学键类型为离子键、共价键.
(5)表中形成两性氢氧化物的元素是Al(用元素符号填写),写出该元素的氢氧化物分别与⑥、⑨的最高价氧化物对应水化物反应的离子方程式:Al(OH)3+3H+═Al3++3H2O,Al(OH)3+OH-═AlO2-+2H2O.
| I A | IIA | ⅢA | IVA | VA | ⅥA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属元素是K,非金属性最强的元素是F(用元素符号填写);
(3)写出⑦和⑨形成的化合物的电子式
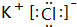
(4)①的氢化物与⑦的氢化物能够发生反应,写成形成盐M的电子式
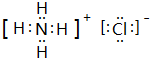 ,M中的化学键类型为离子键、共价键.
,M中的化学键类型为离子键、共价键.(5)表中形成两性氢氧化物的元素是Al(用元素符号填写),写出该元素的氢氧化物分别与⑥、⑨的最高价氧化物对应水化物反应的离子方程式:Al(OH)3+3H+═Al3++3H2O,Al(OH)3+OH-═AlO2-+2H2O.
8.短周期元素Q、W、X、Y、Z在元素周期表中的对应位置如图所示,其中只有Z为金属元素.下列说法正确的是( )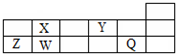

| A. | W、X两元素在自然界中都存在相应的单质 | |
| B. | Q、Y分别与钠元素形成的化合物中仅含离子键 | |
| C. | 简单离子半径由大到小的顺序为:Q>Y>Z | |
| D. | X、Z的最高价氧化物对应的水化物之间易发生化学反应 |
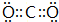 ;
;