题目内容
还原2.4×10-3 mol XO(OH)3+到X元素的低价态时,消耗0.2mol?L-1的Na2SO3溶液30mL,则X元素反应后的价态是( )
| A、+1 | B、-1 | C、0 | D、-2 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:Na2SO3还原2.4×10-3molXO(OH)3+到X元素的低价态,则Na2SO3被氧化为Na2SO4,反应中S元素的化合价由+4价升高为+6价,令X元素在还原产物中的化合价为a,根据电子转移守恒计算a的值.
解答:
解:Na2SO3还原2.4×10-3molXO(OH)3+到X元素的低价态,则Na2SO3被氧化为Na2SO4,反应中S元素的化合价由+4价升高为+6价,
令X元素在还原产物中的化合价为a,
由电子守恒可知,2.4×10-3mol×(6-a)=0.03L×0.2mol?L-1×(6-4),
解得a=1,
故选A.
令X元素在还原产物中的化合价为a,
由电子守恒可知,2.4×10-3mol×(6-a)=0.03L×0.2mol?L-1×(6-4),
解得a=1,
故选A.
点评:本题考查氧化还原反应的有关计算,为高频考点,把握反应中元素的化合价变化及电子守恒为解答的关键,题目难度不大,注意计算中守恒思想的运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在试管的内壁附着下列物质,用稀盐酸浸泡而不能除去的是( )
| A、用足量一氧化碳还原氧化铁后留下的物质 |
| B、用足量氢气还原氧化铜后留下的红色物质 |
| C、盛石灰水后留下的白色固体 |
| D、硫酸铁溶液与氢氧化钠溶液反应后留下的红褐色固体 |
下列离子方程式的书写正确的是( )
| A、AlCl3溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ |
| B、CuSO4溶液中加入过量Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
| C、铜与AgNO3溶液反应:Cu+2Ag+═Cu2++2Ag |
| D、碳酸钙与过量盐酸的反应:CO32-+H+═H2O+CO2↑ |
下列离子在酸性溶液中能大量共存的是( )
| A、S2- NO3- NH4+ K+ |
| B、OH- Na+ Cl- K+ |
| C、NO3- Fe3+ Cl- SO42- |
| D、SO32- H+ K+ NO3- |
下列离子方程式,不正确的是( )
| A、氯水中通入SO2:Cl2+SO2+2H2O=4H++2Cl-+SO42- |
| B、碳酸氢钙溶液中加入过量NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、碳酸氢铵溶液与足量氢氧化钠溶液混合:NH4++HCO3-+2OH-=NH3?H2O+H2O+CO32- |
| D、金属Cu与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
己烯雌酚是一种激素类药物,其结构简式如图所示.下列有关叙述中不正确的是( )
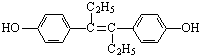

| A、己烯雌酚的分子式为C18H20O2 |
| B、己烯雌酚分子中一定有16个碳原子共平面 |
| C、己烯雌酚为芳香族化合物 |
| D、己烯雌酚可发生加成、取代、氧化、加聚、酯化、硝化反应 |
 (1)在原电池中,通常较活泼的金属做
(1)在原电池中,通常较活泼的金属做