题目内容
有A、B、C、D、E五种原子序数小于18的元素,其特征信息如下:
请回答以下问题:
(1)由A、B、C三种元素形成的化合物含有的化学键类型是 .
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程式 .
(3)D单质与由A、B、C三种元素形成的化合物的水溶液反应的离子方程式 .
(4)写出实验室用软锰矿(MnO2)制取E的化学方程式 .
(5)C和D两元素形成的单质活泼些较强的是 (写元素符号),判断依据是 .
| 元素编号 | 特征信息 |
| A | 其中一种原子核内只有质子没有中子 |
| B | 其原子的L层电子数是K层的3倍 |
| C | 其阳离子与B的阴离子具有相同的电子层结构, 且核电荷数与B相差3 |
| D | 其原子的最外层电子数等于电子层数,且是地壳 中含量较多的元素之一 |
| E | 单质为黄绿色气体,可用于制造漂白粉 |
(1)由A、B、C三种元素形成的化合物含有的化学键类型是
(2)由A、B、C元素中两两组合形成的化合物相互反应生成单质的化学方程式
(3)D单质与由A、B、C三种元素形成的化合物的水溶液反应的离子方程式
(4)写出实验室用软锰矿(MnO2)制取E的化学方程式
(5)C和D两元素形成的单质活泼些较强的是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A其中一种原子核内只有质子没有中子,故A是H;B原子的L层电子数是K层的3倍,故B是O;C阳离子与B的阴离子具有相同的电子层结构,且核电荷数与B相差3,故C是Na;D原子的最外层电子数等于电子层数,且是地壳中含量较多的元素之一,故D是Al;E单质为黄绿色气体,可用于制造漂白粉,故E为Cl,据此解答各小题即可.
解答:
解:(1)由H、O、Na三种元素形成的化合物是氢氧化钠,氢氧化钠中含有离子键和共价键,故答案为:离子键、(极性)共价键;
(2)由H、O、Na元素中两两组合形成的化合物为过氧化钠和水,因为过氧化钠和水能反应生成氧气,反应的方程式为:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑.
(3)Al是两性金属单质,与氢氧化钠反应生成氢气和偏铝酸钠,离子反应方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)实验室中常用二氧化锰与浓盐酸反应制取氯气,化学反应方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(5)比较金属性活泼可以从以下几方面:a.与水是否反应以及反应的剧烈程度;
b.最高价氧化物对应水合物的碱性强弱;
c.原电池中作哪一极,通常负极活泼;
d.单质间的置换顺序,据此比较Na与Al的金属性活泼顺序可以是:金属钠可以和冷水剧烈反应,而铝不可以,故Na活泼,故答案为:Na;金属钠可以和冷水剧烈反应,铝不可以.
(2)由H、O、Na元素中两两组合形成的化合物为过氧化钠和水,因为过氧化钠和水能反应生成氧气,反应的方程式为:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑.
(3)Al是两性金属单质,与氢氧化钠反应生成氢气和偏铝酸钠,离子反应方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)实验室中常用二氧化锰与浓盐酸反应制取氯气,化学反应方程式为:MnO2+4HCl(浓)
| ||
| ||
(5)比较金属性活泼可以从以下几方面:a.与水是否反应以及反应的剧烈程度;
b.最高价氧化物对应水合物的碱性强弱;
c.原电池中作哪一极,通常负极活泼;
d.单质间的置换顺序,据此比较Na与Al的金属性活泼顺序可以是:金属钠可以和冷水剧烈反应,而铝不可以,故Na活泼,故答案为:Na;金属钠可以和冷水剧烈反应,铝不可以.
点评:本题主要考查的是元素及其化合物的推断,属于高考常考题,本题较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于浓硫酸和浓硝酸的叙述不正确的是( )
| A、加热条件下均能与碳反应 |
| B、长期露置在空气中浓度均会降低 |
| C、常温下均不能用铁制容器贮存 |
| D、一定条件下均可与铜片反应 |
设阿伏伽德罗常数的值为NA,下列结论错误的是( )
| A、完全电解2molH2O断裂的σ键键数为4NA |
| B、标准状况下,11.2LCO2中含有的π键键数为2 NA |
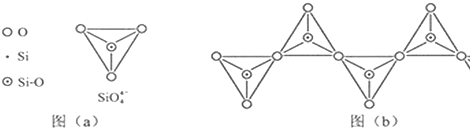
| C、60gSiO2晶体中含有的Si-O键键数为4NA |
| D、12g金刚石中含有C-C键键数为2NA |

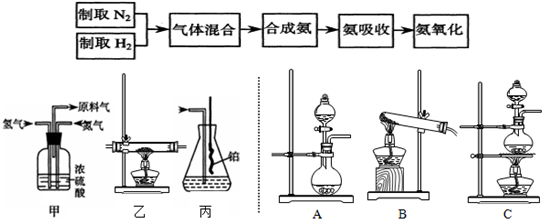
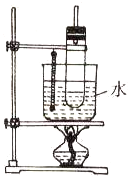 实验室制取硝基苯常用如图装置:
实验室制取硝基苯常用如图装置: