题目内容
6.某二元酸(化学式用H2B表示)水溶液电离是:H2B?H++HB- HB-?H++B2-.回答下列问题:(6)在0.1 mol/L的Na2B溶液中,下列粒子浓度关系式正确的是
BC
A.c( B2-)+c(HB-)=0.1 mol/L B.c(Na+)=2( c( B2-)+c(HB-)+c(H2B))
C.c(OH-)=c(H+)+c(HB-)+2 c(H2B) D.c(Na+)+c(H+)=c(OH-)+c(HB-)+c( B2-)
分析 根据该二元酸的电离方程式知,某二元酸(化学式用H2B表示)水溶液电离是:H2B?H++HB- HB-?H++B2-,所以B2-能够发生两步水解,根据氢离子和氢氧根离子浓度相对大小确定溶液的酸碱性,任何电解质溶液中都存在电荷守恒和物料守恒,据此分析解答
解答 解:A.在0.1 mol/L的Na2B溶液中存在物料守恒,c( B2-)+c(HB-)+c(H2B)=0.1 mol/L,故A错误;
B.据物料守恒可得:c(Na+)=2c(B2-)+2c(HB-)+2c(H2B),故B正确;
C.溶液中存在质子守恒c(OH-)=c(H+)+c(HB-)+2 c(H2B),故C正确;
D.根据电荷守恒可得:c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-),故D错误;
故选BC.
点评 本题考查了盐溶液酸碱性的判断、溶液中离子浓度的关系、难溶物溶解平衡及其计算,题目难度中等,注意掌握判断溶液中离子浓度大小的常用方法,明确电荷守恒、物料守恒的含义及有关难溶物溶度积计算方法.

练习册系列答案
相关题目
16.下列物质只含有共价键的化合物是( )
| A. | N2 | B. | NaOH | C. | H2O | D. | Ar |
17.生产、生活离不开化学.下列说法中不正确的是( )
| A. | 油脂皂化生成的高级脂肪酸钠是肥皂的有效成分 | |
| B. | 加热能杀死甲型 HINI 流感病毒是因为病毒的蛋白质受热变性 | |
| C. | 利用太阳能等能源替代化石能源能改善空气质量 | |
| D. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
14.关于化学反应与能量的说法中错误的是( )
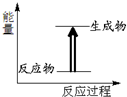

| A. | 如图所示的反应为放热反应 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 需要加热的化学反应不一定是吸热反应 | |
| D. | 化学键断裂吸收能量,化学键生成放出能量 |
1.根据元素周期律和物质结构的有关知识,以下有关排序错误的是( )
| A. | 离子半径:S2->Cl->Ca2+ | B. | 还原性:I->Br->Cl- | ||
| C. | 热稳定性:HCl>H2S>H2Se | D. | 酸性:HClO4<HBrO4<HIO4 |
11.漆器是中华民族传统工艺的瑰宝,常以木材(炭)、金属为胎骨,在胎骨上层层髹红漆.漆的主要成分是含有15或17个碳原子的烷基邻苯二酚.下列说法不正确的是( )
| A. | 收藏漆器工艺品应注意避免阳光暴晒 | |
| B. | “钻石恒久远,一颗永流传”中的钻石和漆器中的木炭均由碳元素组成 | |
| C. | 铜做胎骨的漆器,掉漆后长时间放置,铜的表面仍能保持光亮 | |
| D. | 漆的烷基部分碳原子数越多越难溶于水 |
15.下列各组中两个化学反应,属于同一反应类型的一组是( )
| A. | 由苯制硝基苯;由苯制环己烷 | |
| B. | 由乙烯制1,2-二溴乙烷;由乙烷制一氯乙烷 | |
| C. | 乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 由苯制溴苯;CH4制CH2Cl2 |
16.下列物质属于烷烃的是( )
| A. | CH3CH2OH | B. | CO | C. | 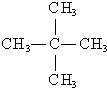 | D. | CH2═CH-CH3 |