题目内容
分析推理是化学学习的方法之一.下列实验推理中,正确的是( )
| A、金属的冶炼方法与金属的活泼性有很大关系,所以银和汞可以用热分解的方法冶炼 |
| B、钠比铜活泼,所以钠可以从硫酸铜溶液中置换出铜 |
| C、工业上电解熔融氯化镁可制得金属镁,所以工业上电解熔融氯化铝可制得铝 |
| D、将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡,说明镁比铝活泼 |
考点:金属冶炼的一般原理,常见金属元素的单质及其化合物的综合应用
专题:元素及其化合物
分析:A.根据金属的活动性强弱选择合适的冶炼方法,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼;
B.钠可以与硫酸铜溶液反应,但先发生Na与水的反应;
C.工业上电解熔融氯化镁可制得金属镁,AlCl3为共价化合物,工业上电解熔融氧化铝可制得铝;
D.将镁条和铝片用导线连接再插进稀NaOH溶液,构成原电池,Al作负极;
B.钠可以与硫酸铜溶液反应,但先发生Na与水的反应;
C.工业上电解熔融氯化镁可制得金属镁,AlCl3为共价化合物,工业上电解熔融氧化铝可制得铝;
D.将镁条和铝片用导线连接再插进稀NaOH溶液,构成原电池,Al作负极;
解答:
解:A.根据金属的活动性强弱选择合适的冶炼方法,Hg、Ag等金属都是不活泼金属,所以应采用用加热分解氧化物的方法冶炼,故A正确;
B.钠可以与硫酸铜溶液反应,先发生Na与水的反应,生成的碱再与盐溶液反应,不会置换出金属Cu,故B错误;
C.工业上可用电解氯化镁的方法制金属镁,其反应的原理是:MgCl2
Mg+Cl2↑,熔融AlCl3中没有离子,不能导电,工业上电解熔融氧化铝2Al2O3
4Al+3O2↑,故C错误;
D.镁比铝活泼,但由于镁和氢氧化钠溶液不反应,而铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,则铝为负极,镁为正极,正极上有气体生成,故D错误;
故选A.
B.钠可以与硫酸铜溶液反应,先发生Na与水的反应,生成的碱再与盐溶液反应,不会置换出金属Cu,故B错误;
C.工业上可用电解氯化镁的方法制金属镁,其反应的原理是:MgCl2
| ||
| ||
| 冰晶石 |
D.镁比铝活泼,但由于镁和氢氧化钠溶液不反应,而铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,则铝为负极,镁为正极,正极上有气体生成,故D错误;
故选A.
点评:本题考查金属元素化合物的性质,侧重考查金属的冶炼,D选项明确电池的工作原理以及原电池的组成是解答该的关键,注重基础知识的考查,题目难度不大,注意铝与氢氧化钠溶液反应的特点.

练习册系列答案
相关题目
下列说法正确的是( )
| A、2mol的盐酸 |
| B、0.1mol氢 |
| C、0.3molHCl |
| D、4mol的氧元素 |
下列变化不能用勒夏特列原理解释的是( )
| A、向H2S水溶液中加入NaOH有利于S2-增多 |
| B、H2、I2、HI混合气体加压后颜色变深 |
| C、合成氨时将氨液化分离,可提高原料的利用率 |
| D、新制氯水久置后颜色变浅 |
天然气根据成分不同分为贫气和富气,贫气中甲烷的含量较多,富气中乙烷、丙烷、丁烷的含量相对高一些.若要将它们液化,下列说法正确的是( )
| A、贫气易液化 |
| B、富气易液化 |
| C、二者液化条件相同 |
| D、加压降温均有利于两者液化 |
已知有如下反应:Cl2+2I-=2Cl-+I2;Cl2+2Fe2+=2Cl-+2Fe3+;2Fe3++2I-=I2+2Fe2+;I2+SO2+2H2O=2I-+SO42-+4H+,下列叙述正确的是( )
| A、该反应是不可能发生的:Cl2+SO2+2H2O=2Cl-+SO42-+4H+ |
| B、氧化性:Cl2>Fe3+>I2 |
| C、还原性:I->Cl->Fe2+ |
| D、将SO2通入FeCl3溶液中得不到 SO42- |
已知25℃时几种弱酸的电离平衡常数:
则下列有关说法正确的是( )
| 弱酸 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.7×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、相同浓度的CH3COONa和NaClO的混合溶液中:C(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
| B、pH相等的CH3COONa、NaClO和Na2CO3溶液:c(NaClO)<c(CH3COONa)<c(Na2CO3) |
| C、amol/L HClO溶液与bmol/L NaOH溶液等体积混合后,所得溶液中:c(Na+)>c(ClO-),则b一定大于a |
| D、向0.1mol/L CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液的pH=5 |
下列表达方式错误的是( )
A、碳-12原子构成
| ||
B、CO2的分子模型示意图: | ||
| C、S2-的核外电子排布式 1s22s22p63s23p6 | ||
D、甲烷的电子式 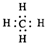 |