题目内容
现有氯化钾和硝酸钾的固体混合物50 g,其中氯化钾的质量分数为10%.试说明从KCl和KNO3的混合物中提纯KNO3的实验方法和实验原理以及具体实验方案.
解析:
|
答案:(1)实验方法:溶解、冷却结晶. (2)实验原理:KCl和KNO3的溶解度曲线如图:
从上可知:混合物中,KNO3的溶解度受温度影响变化较大,而KCl的溶解度受温度影响相对较小,故KCl和KNO3的分离提纯可以用先溶解、再冷却结晶的方法来实现. (3)实验方案:KCl和KNO3的分离提纯可以使用结晶的方法. 由于混合物中KNO3含量较高(90%),可首先配制较高温度(如100℃)下的KNO3饱和溶液,利用降温结晶的方法,使KNO3晶体在较低温度下析出,此时KCl不析出. 实验中加入水的量可根据混合物中KNO3的质量和较高温度下KNO3的溶解度进行计算(使KNO3恰好溶解),如100℃时,KNO3溶解度为246 g,则有: ①溶解:将50 g KCl和KNO3的混合物放入烧杯中,然后加入约18.3 mL 100℃的热水,用玻璃棒搅拌,使固体完全溶解. ②降温结晶:将(1)所得溶液放在实验台上自然冷却至不再有固体析出. ③过滤:将(2)所得混合物进行过滤,滤纸上晶体即为较纯净的KNO3. ④重结晶:若需要更纯净的KNO3晶体,可将(3)中所得KNO3晶体再结晶(重复①~③操作)一次. 解析:KCl和KNO3均能溶解于水.其中KNO3的溶解度受温度影响变化较大,而KCl的溶解度受温度的影响相对较小,故可采用冷却降温结晶的方法分离提纯出KNO3晶体,而让KCl不析出,而留在溶液中,再过滤出KNO3晶体. |
提示:
|
(1)重结晶又叫再结晶,即使晶体重复结晶,以进一步分离或提纯混合物. (2)步骤③的滤液若进行蒸发结晶并趁热过滤,所得晶体将是较纯净的KCl,从而可以实现KNO3和KCl混合物的分离. |

 教材全解字词句篇系列答案
教材全解字词句篇系列答案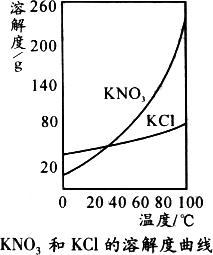
 无土栽培是利用营养液栽培作物的一种方法.现有一种无色的营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验.
无土栽培是利用营养液栽培作物的一种方法.现有一种无色的营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验.

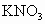 混合物中提纯
混合物中提纯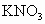 混合物中提纯
混合物中提纯