题目内容
5.向下列各物质的水溶液中滴加稀硫酸或MgCl2溶液时,均有白色沉淀生成的是( )| A. | Ba(NO3)2 | B. | KOH | C. | Ba(OH)2 | D. | Na2CO3 |
分析 向下列各物质的水溶液中滴加稀硫酸或MgCl2溶液时,均有白色沉淀生成,说明硫酸中形成的沉淀为硫酸钡沉淀,证明溶液中含钡离子,滴加氯化镁溶液中生成白色沉淀可能为AgCl或Mg(OH)2,试剂中应含银离子或氢氧根离子,结合硫酸溶液中生成硫酸钡沉淀和选项试剂分析试剂的组成.
解答 解:向下列各物质的水溶液中滴加稀硫酸或MgCl2溶液时,均有白色沉淀生成,说明硫酸中形成的沉淀为硫酸钡沉淀,证明溶液中含钡离子,滴加氯化镁溶液中生成白色沉淀可能为AgCl或Mg(OH)2,试剂中应含银离子或氢氧根离子,分析判断溶液中应含钡离子和氢氧根离子满足反应现象,
A.加入硫酸生成白色沉淀,加入氯化镁无沉淀生成,故A错误;
B.加入氢氧化钾硫酸溶液中无沉淀生成,故B错误;
C.加入氢氧化钡溶液中符合滴加稀硫酸或MgCl2溶液时,均有白色沉淀生成,故C正确;
D.碳酸钠溶液中加入硫酸雾沉淀生成,故D错误;
故选C.
点评 本题考查了离子性质,反应现象的分析判断,主要是形成沉淀离子的理解应用,题目难度中等.

练习册系列答案
相关题目
10.在标准状况下,下列物质中体积最大的是( )
| A. | 22.4 L H2 | B. | 含3.01×1023 个分子的Cl2 | ||
| C. | 10g NH3 | D. | 0.8 mol SO2 |
11.下列关于实验室制取SO2的实验,其中叙述正确的是( )
| A. | 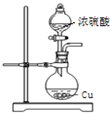 可用图中装置和药品制取SO2 | |
| B. | 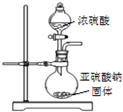 可用图中装置和药品制取SO2 | |
| C. | 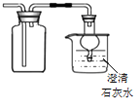 可用图中装置和药品收集二氧化硫并吸收尾气 | |
| D. | 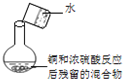 可用图中装置和药品检验铜和浓硫酸反应生成的CuSO4 |
13.往蛋白质溶液里加入下列物质会产生沉淀,但再加水稀释,沉淀又会溶解的是( )
| A. | CuSO4 | B. | CH3CH2OH | C. | Na2SO4 | D. | NH4CI |
20.下列图示与对应的叙述相符的是( )
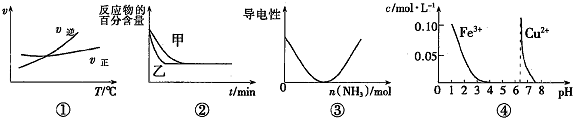

| A. | 据图①可判断可逆反应A2(g)+3B2(g)?2AB3(g)的△H>0 | |
| B. | 图②表示压强对可逆反应2A(g)+B(g)?3C(g)+D(s)的影响,乙的压强大 | |
| C. | 图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 | |
| D. | 据图④,若除去0.1 mol•L-1CuSO4溶液中混有的Fe3+,可向溶液中加入适量NaOH至pH约为7 |
10.在溶液中能大量共存的一组离子是( )
| A. | NH4+、H+、NO3-、HCO3- | B. | K+、Ag+、NO3-、Cl- | ||
| C. | H+、K+、SO42-、CH3COO- | D. | Na+、Cl-、CO32-、OH- |
17.下列变化属于化学变化的是( )
| A. | 过滤除去水中的泥沙 | B. | 食物腐烂 | ||
| C. | 蒸馏法分离酒精与水 | D. | 分液法分离四氯化碳与水 |
15.下列操作或装置能达到实验目的是( )
| A. | 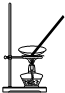 灼烧 灼烧 | B. | 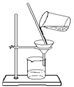 分离Fe(OH)3胶体 分离Fe(OH)3胶体 | ||
| C. | 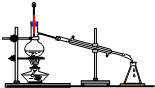 制备蒸馏水 制备蒸馏水 | D. | 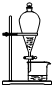 分离酒精和水 分离酒精和水 |
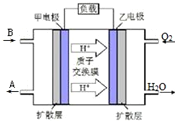 已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系.
已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系.