题目内容
为测定某碳酸氢钠样品纯度(含有少量氯化钠),学生设计了如下几个实验方案(每个方案均称取m1g样品),请回答每个方案中的问题.

[方案Ⅰ]选用重量法进行测定:可用如图1中的装置进行实验.
(1)A装置中NaOH溶液的作用是 若直接向试样溶液中鼓入空气会导致实验测定结果 (填“偏高”、“偏低”或“无影响”).
(2)该方案需直接测定的物理量是 .
[方案Ⅱ]选用气体体积法进行测定:可用如图2中的装置进行实验,为了减小实验误差,量气管中加入饱和NaHCO3溶液.
(3)通过实验,测得该试样中碳酸氢钠质量分数偏低,产生这种现象的原因可能是 .
a.测定气体体积时未冷却至室温
b.测定气体体积时水准管的液面高于量气管的液面
c.Y型管中留有反应生成的气体
d.气体进入量气管前未用浓硫酸干燥
[方案Ⅲ]选用滴定法进行测定:
(4)称取m1g样品,配成100mL溶液,取出20mL,用c mol?L-1的标准HCl溶液滴定,消耗体积为VmL,则该试样中碳酸氢钠质量分数的计算表达式为: .

[方案Ⅰ]选用重量法进行测定:可用如图1中的装置进行实验.
(1)A装置中NaOH溶液的作用是
(2)该方案需直接测定的物理量是
[方案Ⅱ]选用气体体积法进行测定:可用如图2中的装置进行实验,为了减小实验误差,量气管中加入饱和NaHCO3溶液.
(3)通过实验,测得该试样中碳酸氢钠质量分数偏低,产生这种现象的原因可能是
a.测定气体体积时未冷却至室温
b.测定气体体积时水准管的液面高于量气管的液面
c.Y型管中留有反应生成的气体
d.气体进入量气管前未用浓硫酸干燥
[方案Ⅲ]选用滴定法进行测定:
(4)称取m1g样品,配成100mL溶液,取出20mL,用c mol?L-1的标准HCl溶液滴定,消耗体积为VmL,则该试样中碳酸氢钠质量分数的计算表达式为:
考点:探究物质的组成或测量物质的含量,钠的重要化合物
专题:实验探究和数据处理题
分析:(1)本题是通过碳酸氢钠与硫酸反应生成二氧化碳,再用碱石灰吸收二氧化碳,通过二氧化碳的质量求碳酸氢钠的质量分数,故应排除空气中二氧化碳的干扰,若不吸收空气中的二氧化碳会导致测定结果偏高.
(2)需要直接测定的物理量是装置C反应前后的质量,其质量差即为二氧化碳的质量.
(3)a项会使测定结果偏高;b项气体压强大于大气压,会使测定的体积偏小,导致碳酸氢钠的测定结果偏低;c项,原Y形管内有空气,后留有反应产生的气体不影响实验结果;本题是用排水集气法测定气体体积,不需要干燥,d项无影响.
(4)根据化学方程式:NaHCO3+HCl═NaCl+CO2↑+H2O,可知反应消耗的盐酸与碳酸氢钠的物质的量相等.
(2)需要直接测定的物理量是装置C反应前后的质量,其质量差即为二氧化碳的质量.
(3)a项会使测定结果偏高;b项气体压强大于大气压,会使测定的体积偏小,导致碳酸氢钠的测定结果偏低;c项,原Y形管内有空气,后留有反应产生的气体不影响实验结果;本题是用排水集气法测定气体体积,不需要干燥,d项无影响.
(4)根据化学方程式:NaHCO3+HCl═NaCl+CO2↑+H2O,可知反应消耗的盐酸与碳酸氢钠的物质的量相等.
解答:
解:(1)本题是通过碳酸氢钠与硫酸反应生成二氧化碳,再用碱石灰吸收二氧化碳,通过二氧化碳的质量求碳酸氢钠的质量分数,故应排除空气中二氧化碳的干扰,若不吸收空气中的二氧化碳会导致测定结果偏高;故答案为:吸收空气中的CO2;偏高;
(2)本题是通过碳酸氢钠与硫酸反应生成二氧化碳,再用碱石灰吸收二氧化碳,通过二氧化碳的质量来计算碳酸氢钠的质量,故需要直接测定的物理量是装置C反应前后的质量,其质量差即为二氧化碳的质量;故答案为:装置C反应前后的质量;
(3)a项:测定气体体积时未冷却至室温,由于热胀冷缩,导致所测体积偏大,会使测定结果偏高;b项气体压强大于大气压,会使测定的体积偏小,导致碳酸氢钠的测定结果偏低;c项,原Y形管内有空气,后留有反应产生的气体不影响实验结果;本题是用排水集气法测定气体体积,不需要干燥,d项无影响;故选b;
(4)碳酸氢钠和盐酸反应方程式:
NaHCO3+HCl═NaCl+CO2↑+H2O,
84g 1mol
m cmol/L×VmL×10-3L/mol
m=×
=84cV×10-3g,
碳酸氢钠的质量分数为:
×100%.
故答案为:
×100%.
(2)本题是通过碳酸氢钠与硫酸反应生成二氧化碳,再用碱石灰吸收二氧化碳,通过二氧化碳的质量来计算碳酸氢钠的质量,故需要直接测定的物理量是装置C反应前后的质量,其质量差即为二氧化碳的质量;故答案为:装置C反应前后的质量;
(3)a项:测定气体体积时未冷却至室温,由于热胀冷缩,导致所测体积偏大,会使测定结果偏高;b项气体压强大于大气压,会使测定的体积偏小,导致碳酸氢钠的测定结果偏低;c项,原Y形管内有空气,后留有反应产生的气体不影响实验结果;本题是用排水集气法测定气体体积,不需要干燥,d项无影响;故选b;
(4)碳酸氢钠和盐酸反应方程式:
NaHCO3+HCl═NaCl+CO2↑+H2O,
84g 1mol
m cmol/L×VmL×10-3L/mol
m=×
| 84g×cmol/L×VmL×10-3L/mol |
| 1mol |
碳酸氢钠的质量分数为:
84cV×10-3g×
| ||
| m1g |
故答案为:
84cV×10-3g×
| ||
| m1g |
点评:本题考查较为综合,为高考常见题型,侧重于学生的分析能力、计算能力和实验能力的考查,注意把握物质的性质以及反应的实验原理,难度中等.通过本题我们要知道在完成实验时要尽可能的排除可能对实验结果产生影响的因素,例如本题中空气中二氧化碳对实验结果的影响,水蒸气的影响等.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
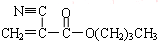 ).
).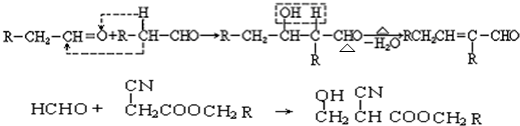
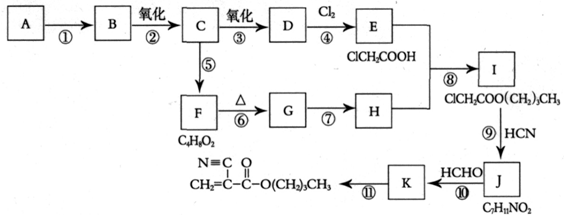
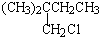 ,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如所示.
,B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如所示.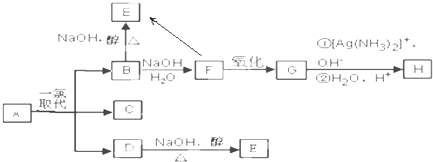

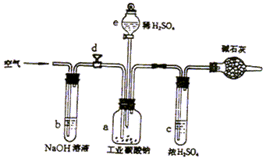 工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如图的装置:
工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如图的装置: