��Ŀ����
��16�֣�����2 L�ܱ������н��з�Ӧ��mX(g)+nY(g) 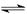 pZ(g)+qQ(g),ʽ��m��n��p��qΪ����ϵ������0 min��3 min �ڣ����������ʵ����ı仯���±���ʾ��
pZ(g)+qQ(g),ʽ��m��n��p��qΪ����ϵ������0 min��3 min �ڣ����������ʵ����ı仯���±���ʾ��
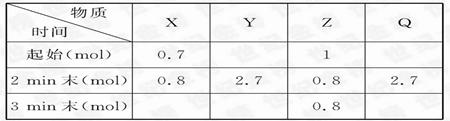
��֪2 min�� v(Q)="0.075" mol��L-1��min-1,�� v(z)��v(Y)=1:2
(1)��ȷ���������ʵ����������ʼʱn(Y)=________��n(Q)=_________��
(2)����ʽ��m =______��n =______��p=______��q=_______��
(3)��Z��ʾ2 min�ڵķ�Ӧ����_____________��
(4)2 minĩQ��ת����Ϊ_____________
(5)���ж���2 min��v������______v���棩(�>������<����=��)����2 minĩ��3 minĩv������_____ v���棩(�>������<����=��)��
 pZ(g)+qQ(g),ʽ��m��n��p��qΪ����ϵ������0 min��3 min �ڣ����������ʵ����ı仯���±���ʾ��
pZ(g)+qQ(g),ʽ��m��n��p��qΪ����ϵ������0 min��3 min �ڣ����������ʵ����ı仯���±���ʾ��
��֪2 min�� v(Q)="0.075" mol��L-1��min-1,�� v(z)��v(Y)=1:2
(1)��ȷ���������ʵ����������ʼʱn(Y)=________��n(Q)=_________��
(2)����ʽ��m =______��n =______��p=______��q=_______��
(3)��Z��ʾ2 min�ڵķ�Ӧ����_____________��
(4)2 minĩQ��ת����Ϊ_____________
(5)���ж���2 min��v������______v���棩(�>������<����=��)����2 minĩ��3 minĩv������_____ v���棩(�>������<����=��)��
����16�֣���2С��ÿ��1�֣�����ÿ��2�֣�
(1)2.3 mol 3 mol (2)1 4 2 3
(3)0.05 mol��L-1��min-1 (4)10% (5)< =
(1)2.3 mol 3 mol (2)1 4 2 3
(3)0.05 mol��L-1��min-1 (4)10% (5)< =
�����������1�����ݱ������ݿ�֪��2minĩZ���ʵ�Ũ�Ȳ��ٷ����仯�����Է�Ӧ����ƽ��״̬������v(Q)="0.075" mol��L-1��min-1��֪��Q���ʵı仯����0.075 mol��L-1��min-1��2L��2min��0.3mol������Q����ʼ����0.3mol��2.7mol��3.0mol��Z���ʵı仯����0.2mol������p��2��q��3����n��4������ΪX�ı仯����0.1mol������m��1������Y���ʵ����ʵ�����0.1mol��4��0.4mol������Y����ʼ����2.7mol��0.4mol��2.3mol��
��2������1�����
��3��Z���ʵı仯����0.2mol��������Z��ʾ2 min�ڵķ�Ӧ������
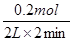 ��0.05 mol��L-1��min-1��
��0.05 mol��L-1��min-1����4��2 minĩQ��ת������0.3��3.0��100����10����
��5����2 min�ڸ÷�Ӧû�дﵽƽ��״̬���������Ǵ������↑ʼ����ƽ��ģ�����v������С��v���棩��2minʱ��Ӧ�ﵽƽ��״̬������v����������v���棩��
�������ڽ��з�Ӧ���ʵ��йؼ���ʱ������Ҫ���÷�Ӧ����֮������Ӧ�Ļ�ѧ������֮����һ��ϵʽ�����йصļ�����жϡ�

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ
 CO��g����H2O��g����
CO��g����H2O��g����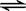 2SO3,��ƽ��ʱSO3Ϊn mol����ͬ�¶��·ֱ��������,ƽ���SO3�����ʵ�������n mol���ǣ� ��
2SO3,��ƽ��ʱSO3Ϊn mol����ͬ�¶��·ֱ��������,ƽ���SO3�����ʵ�������n mol���ǣ� �� Sn2��(aq)��Pb(s)����ϵ��c(Pb2��)��c(Sn2��)�仯��ϵ����ͼ��ʾ�������ж���ȷ���ǣ� ��
Sn2��(aq)��Pb(s)����ϵ��c(Pb2��)��c(Sn2��)�仯��ϵ����ͼ��ʾ�������ж���ȷ���ǣ� ��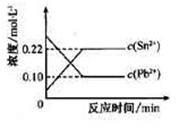
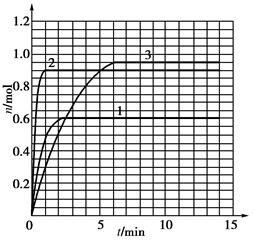
 2NH3(g)(����ӦΪ���ȷ�Ӧ)��Ϊ��ʹƽ�������ɰ��ķ����ƶ����ɲ��õķ�����
2NH3(g)(����ӦΪ���ȷ�Ӧ)��Ϊ��ʹƽ�������ɰ��ķ����ƶ����ɲ��õķ�����