题目内容
某烃的相对分子质量为86,其结构中含有1个-CH2-和4个-CH3,则该烃的二氯代物有( )
| A、5种 | B、6种 | C、7种 | D、8种 |
考点:同分异构现象和同分异构体
专题:同分异构体的类型及其判定
分析:某烃的相对分子质量为86,其结构中含有1个-CH2-和4个-CH3,86-14-15×4=12,说明还有一个碳原子,该烃为C(CH3)3CH2CH3,用定1议2法解题,据此解题.
解答:
解:某烃的相对分子质量为86,其结构中含有1个-CH2-和4个-CH3,86-14-15×4=12,说明还有一个碳原子,该烃为C(CH3)3CH2CH3,二氯代物有: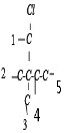 ,
,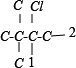 ,
,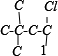 ,共8种,故选D.
,共8种,故选D.
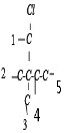 ,
,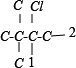 ,
,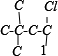 ,共8种,故选D.
,共8种,故选D.
点评:本题考查同分异构体的书写,难度不大,注意二氯代物的书写可以采用定1议2法.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、Cu与FeCl3溶液反应:Cu+Fe3+=Cu2++Fe2+ |
| B、碳酸钙溶于稀盐酸:CO32-+2H+=H2O+CO2↑ |
| C、FeSO4溶液和NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ |
| D、氯气溶于水:Cl2+H2O=2H++ClO-+Cl- |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L H2O含有的分子数为NA |
| B、28g N2和N4组成的混合气体中含有的原子数为2NA |
| C、1mol?L-1 AlCl3溶液中含有的Cl-数目为3NA |
| D、2.3g Na与足量水反应,转移的电子数目为0.2NA |
能正确表示下列反应的离子方程式是( )
A、实验室用大理石和稀盐酸制取CO2:2H++C
| ||
| B、金属钠与足量水反应:Na+2H2O=Na++H2↑+2OH- | ||
C、氢氧化钡溶液中加入稀硫酸:Ba2++S
| ||
| D、Cl2与水反应:Cl2+H2O=H++Cl-+HClO |
为探究原电池的形成条件和反应原理,某同学设计了如下实验步骤并记录了现象:
①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
②向上述稀硫酸中插入铜片,没有看到有气泡生成;
③将锌片与铜片上端接触并捏住,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;
④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转.
下列关于以上实验设计及现象的分析,正确的是( )
①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
②向上述稀硫酸中插入铜片,没有看到有气泡生成;
③将锌片与铜片上端接触并捏住,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;
④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转.
下列关于以上实验设计及现象的分析,正确的是( )
| A、实验①、②说明锌能与稀硫酸反应而铜不能 |
| B、实验③说明发生原电池反应时会加快化学反应速率 |
| C、实验③说明在该条件下铜可以与稀硫酸反应生成氢气 |
| D、实验④说明该原电池中锌为正极、铜为负极 |
下列反应的离子方程式正确的是( )
| A、铜和稀盐酸反应:Cu+2H+=Cu2++H2↑ | ||
B、碳酸氢钠溶于盐酸反应:CO
| ||
| C、钠与水反应:Na+H2O=Na++OH-+H2↑ | ||
D、Ba(OH)2溶液与H2SO4溶液反应:Ba2++2H++2OH-+SO
|

