题目内容
交警常用“司机饮酒检测仪”检查司机是否酒后驾车,其原理是硫酸酸化的重铬酸盐(Cr2O72-橙红色)和乙醇反应生成铬盐(Cr3+绿色)和乙酸等.重铬酸钠(Na2Cr2O7)在工业中有很广泛的应用,常用来制备金属铬.方法如下:
将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬.请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是 .
(2)写出碳和重铬酸钠高温反应的化学方程式 .
(3)写出Cr2O3经铝热法还原制得金属铬的化学方程式是 .
(4)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是 .
(5)某Na2Cr2O7样品2.00g恰好和4.56gFeSO4完全反应,该样品的纯度为 .
将铬铁矿[主要成分Fe(CrO2)2]与纯碱、氧气高温焙烧,除杂、酸化,得到重铬酸钠,碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,Cr2O3再经铝热法还原,即可制得金属铬.请回答:
(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式是
(2)写出碳和重铬酸钠高温反应的化学方程式
(3)写出Cr2O3经铝热法还原制得金属铬的化学方程式是
(4)硫酸酸化的Na2Cr2O7和FeSO4反应,生成Cr3+等,该反应的离子方程式是
(5)某Na2Cr2O7样品2.00g恰好和4.56gFeSO4完全反应,该样品的纯度为
考点:乙醇的化学性质,化学方程式的有关计算,氧化还原反应
专题:计算题,氧化还原反应专题
分析:(1)由于K2Cr2O7在酸性条件下有很强的氧化性,而乙醇具有还原性,能够被氧化成CH3COOH;
(2)由题意可知碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,结合反应中氧化剂和还原剂得失电子守恒,原子个数守恒配平方程式;
(3)三氧化二铬与铝在高温条件下发生置换反应生成铬与三氧化二铝;
(4)Na2Cr2O7和在酸性环境下具有强的氧化性,能够将亚铁离子氧化成三价铁离子,本身被还原生成三价铬离子;
(5)依据方程式Na2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+7H2O+Na2SO4计算解答.
(2)由题意可知碳和重铬酸钠在高温下反应生成Cr2O3、Na2CO3和CO,结合反应中氧化剂和还原剂得失电子守恒,原子个数守恒配平方程式;
(3)三氧化二铬与铝在高温条件下发生置换反应生成铬与三氧化二铝;
(4)Na2Cr2O7和在酸性环境下具有强的氧化性,能够将亚铁离子氧化成三价铁离子,本身被还原生成三价铬离子;
(5)依据方程式Na2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+7H2O+Na2SO4计算解答.
解答:
解:(1)硫酸酸化的K2Cr2O7和乙醇反应的化学方程式为:3C2H6O+2K2Cr2O7+8H2SO4=3CH3COOH+2Cr2(SO4)3+11H2O+2K2SO4;
故答案为:3C2H6O+2K2Cr2O7+8H2SO4=3CH3COOH+2Cr2(SO4)3+11H2O+2K2SO4;
(2)碳和重铬酸钠高温反应的化学方程式为:Na2Cr2O7)+2C
Cr2O3+Na2CO3+CO↑;
故答案为:Na2Cr2O7)+2C
Cr2O3+Na2CO3+CO↑;
(3)三氧化二铬与铝发生铝热反应的方程式为:Cr2O3+2Al
2Cr+Al2O3;
故答案为:Cr2O3+2Al
2Cr+Al2O3 ;
(4)Na2Cr2O7和在酸性环境下与FeSO4反应的离子方程式:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
故答案为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
(5)依据方程式Na2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+7H2O+Na2SO4可知:
Na2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+7H2O+Na2SO4
262 6×152
m 4.56g
则m=1.31g;
Na2Cr2O7样品的百分含量:
×100%=65.5%;
故答案为:65.5%.
故答案为:3C2H6O+2K2Cr2O7+8H2SO4=3CH3COOH+2Cr2(SO4)3+11H2O+2K2SO4;
(2)碳和重铬酸钠高温反应的化学方程式为:Na2Cr2O7)+2C
| ||
故答案为:Na2Cr2O7)+2C
| ||
(3)三氧化二铬与铝发生铝热反应的方程式为:Cr2O3+2Al
| ||
故答案为:Cr2O3+2Al
| ||
(4)Na2Cr2O7和在酸性环境下与FeSO4反应的离子方程式:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
故答案为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
(5)依据方程式Na2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+7H2O+Na2SO4可知:
Na2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+7H2O+Na2SO4
262 6×152
m 4.56g
则m=1.31g;
Na2Cr2O7样品的百分含量:
| 1.31g |
| 2.00g |
故答案为:65.5%.
点评:本题以司机饮酒检测仪原理为载体考查了物质的性质、氧化还原方程式的书写及有关化学方程式的计算,题目难度较大,解题关键在于熟悉各种物质的性质,掌握氧化还原方程式配平方法.

练习册系列答案
相关题目
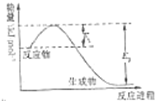 氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题: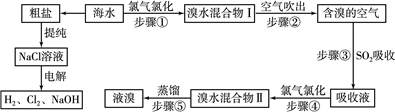
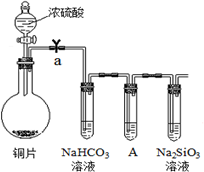 下表是元素周期表的一部分,表中所列字母分别代表一种元素.
下表是元素周期表的一部分,表中所列字母分别代表一种元素.