题目内容
7.R元素的单质4.5g,跟足量的硫酸反应R2(SO4)3并放出5.6L的H2(标准状况).试求:
(1)R的相对原子质量为27;
(2)若R原子中质子数比中子数少1,则R是Al(填元素符号),它在元素周期表中的位置为第三周期第ⅢA族.
分析 (1)根据单质和稀硫酸的反应中电子转移守恒,确定R元素原子的相对原子质量;
(2)相对原子质量在数值上近似等于质量数,据A=Z+N来确定质子数,确定元素原子的核外电子排布以确定该元素在周期表中的位置.
解答 解:(1)设4.5gR元素单质的物质的量为n,根据电子转移守恒,则:
n×3=$\frac{5.6L}{22.4L/mol}$×2,解得n=$\frac{5}{30}$mol,
所以R的摩尔质量M=$\frac{m}{n}$=$\frac{4.5g}{\frac{5}{30}mol}$=27g/mol,
所以R元素的相对原子质量为27,
故答案为:27;
(2)若R原子中质子数比中子数少1,Z+N=Z+Z+1=27,Z=13,R是Al,位于第三周期第ⅢA族,
故答案为:Al;三;ⅢA.
点评 本题考查学生相对原子质量的计算和原子结构决定元素的位置,关键在于运用电子转移守恒计算,难度不大.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
15.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 某溶液中加入硝酸银溶液,产生白色沉淀,该溶液中一定含有Cl- |
2.设阿伏加德罗常数的值为NA,下列说法不正确的是( )
| A. | 18gH218O与D2O的混合物中所含中子数为9NA | |
| B. | 60g HCHO和CH3COOH的混合物中存在的共用电子对总数为8NA | |
| C. | 反应N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3中,当净生成0.2mol NH3生产时,在正反应中N2得到0.6NA电子 | |
| D. | 电解精炼铜中,当阴极增重3.2g时,阳极失去电子0.1NA |
12.下面是四种元素的基态原子的电子排布式,其中化合价最高的是( )
| A. | 1s22s22p3 | B. | 1s22s22p63s23p63d34s2 | ||
| C. | 1s22s22p63s23p6 | D. | 1s22s22p5 |
19.一定温度下,某容器中加入足量碳酸钙,发生反应CaC03(s)=CaO(s)+CO2(g)达到平衡.下列说法正确的是( )
| A. | 将体积缩小为原来的一半,当体系再次达到平衡时,C02的浓度为原来的2倍 | |
| B. | CaCO3(s)加热分解生成Ca0(s)和C02,△s<0 | |
| C. | 将体积增大为原来的2倍,再次达到平衡时,气体密度不变 | |
| D. | 保持容器体积不变,充入He,平衡向逆反应方向进行. |
15.银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故.根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去.下列说法正确的是( )
| A. | 处理过程中银器一直保持恒重 | |
| B. | 银器为正极,Ag2S被氧化生成单质银 | |
| C. | 该过程中总反应为2Al+3Ag2S═6Ag+Al2S3 | |
| D. | 黑色褪去的原因是黑色Ag2S转化为白色Ag |
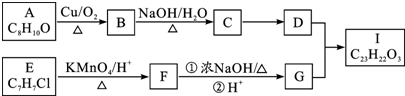
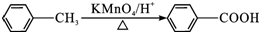
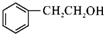 ,C→D的反应类型为加成反应,F中不含氧的官能团的名称为氯原子,I的结构简式为
,C→D的反应类型为加成反应,F中不含氧的官能团的名称为氯原子,I的结构简式为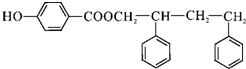 .
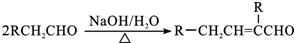
. ,F→G①的化学方程式为
,F→G①的化学方程式为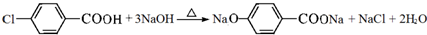 .
.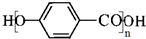 .
.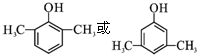 .
. 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.