题目内容
2.苯的分子式为C6H6,结构简式_ 其中碳的质量分数为$\frac{1}{13}$.碳碳键之间的夹角为1200.碳环呈平面正六边形结构,环上的碳碳之间的键完全相同.
其中碳的质量分数为$\frac{1}{13}$.碳碳键之间的夹角为1200.碳环呈平面正六边形结构,环上的碳碳之间的键完全相同.
分析 根据1个苯分子中含6个C、6个H原子,为平面正六边形结构,其中6个碳原子之间的键完全相同,是介于碳碳单键、碳碳双键之间的一种特殊化学键,键角为120°.
解答 解:1个苯分子中含6个C、6个H原子,分子式为C6H6,结构简式 ,其中碳的质量分数为$\frac{1}{13}$,碳碳键之间的夹角为1200,碳环呈平面正六边形结构;
,其中碳的质量分数为$\frac{1}{13}$,碳碳键之间的夹角为1200,碳环呈平面正六边形结构;
故答案为:C6H6; ;$\frac{1}{13}$;1200;平面正六边形.
;$\frac{1}{13}$;1200;平面正六边形.
点评 本题考查苯的结构,应注意的是苯中的键完全相同,均为介于单双键之间的特殊的键.

练习册系列答案
相关题目
13.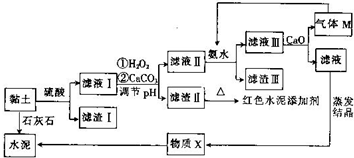 土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.
土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.
已知:黏土的主要成分为2CaO•3Al2O3•FeO•Fe2O3•10SiO2•nH2O.部分难溶物开始沉淀时和完全沉淀时的pH如表所示.
(1)为提高酸浸速率,除适当增大硫酸浓度外,还可采取的措施有搅拌、适当升温或将研磨黏土(任写一条).
(2)向滤液Ⅰ中加入H2O2的作用是将滤液中的Fe2+氧化为Fe3+;用CaCO3调节溶液pH约为3.3,其目的是使Fe3+完全转化为Fe(OH)3沉淀而除去.
(3)红色水泥添加剂的主要成分是Fe2O3.
(4)物质X的化学式为CaSO4•2H2O.
(5)气体M的电子式为 ;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).
;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).
(6)氮化铝广泛用于电子陶瓷等工业领域,以滤渣Ⅲ、碳及氮气为原料可制备氮化铝,用化学方程式表示制备过程:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO.
 土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.
土壤是人类赖以生存的最基本物质,以黏土为原料生产的产品伴随着人类文明的脚步.皖北名胜皇藏峪的黏土,水浸不塌,是生产无机非金属材料的优质原料.某兴趣小组以当地黏土为原料探究彩色水泥、轻质耐火材料的联合生产,其设计的流程如图所示.已知:黏土的主要成分为2CaO•3Al2O3•FeO•Fe2O3•10SiO2•nH2O.部分难溶物开始沉淀时和完全沉淀时的pH如表所示.
| Fe(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 开始沉淀时的pH | 6.3 | 1.9 | 3.4 |
| 完全沉淀时的pH | 8.3 | 3.2 | 4.7 |
(2)向滤液Ⅰ中加入H2O2的作用是将滤液中的Fe2+氧化为Fe3+;用CaCO3调节溶液pH约为3.3,其目的是使Fe3+完全转化为Fe(OH)3沉淀而除去.
(3)红色水泥添加剂的主要成分是Fe2O3.
(4)物质X的化学式为CaSO4•2H2O.
(5)气体M的电子式为
 ;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).
;向滤液Ⅲ中加放CaO的作用是与水反应放热,降低NH3的溶解度(任写一条).(6)氮化铝广泛用于电子陶瓷等工业领域,以滤渣Ⅲ、碳及氮气为原料可制备氮化铝,用化学方程式表示制备过程:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO.
17.某有机物在氧气中充分燃烧,生成的二氧化碳和水的物质的量之比为1:1,由此可得出的正确结论是( )
| A. | 该有机物分子中碳、氢、氧原子个数比为1:2:3 | |
| B. | 该有机物分子中碳、氢原子个数比为1:2 | |
| C. | 该有机物中肯定含氧 | |
| D. | 可以判断该有机物中是否含氧 |
7.已知反应4P+3KOH+3H2O═3KH2PO2+PH3↑,下列说法正确的是( )
| A. | P被氧化 | B. | KOH是还原剂,P是氧化剂 | ||
| C. | P既被氧化又被还原 | D. | KH2PO2是还原产物,PH3是氧化产物 |
14.北京和张家口市联合申办2022年冬奥会,目前北京市政府正在全力改善空气质量.以下不在空气质量报告范围内的是( )
| A. | 二氧化硫(SO2) | B. | 总悬浮颗粒物(TSP) | C. | 二氧化氮(NO2) | D. | 二氧化碳(CO2) |
11.将等物质的量的下列物质露置于空气中,最后质量变化由小到达的顺序是( )
①Na ②Na2O ③Na2O2 ④NaOH ⑤Na2CO3.
①Na ②Na2O ③Na2O2 ④NaOH ⑤Na2CO3.
| A. | ⑤<④<③<①<② | B. | ②<①<③<④<⑤ | C. | ⑤<④<②=③<① | D. | ⑤<③<④<②<① |