题目内容
12.铁是生活中的一种常见金属,用途非常广泛.(1)FeCl3溶液用于腐蚀印刷线路板,反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+
(2)用废铁皮制取铁红粉的局部流程图如下:
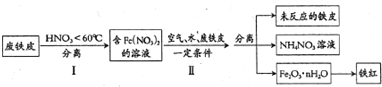
①步骤I温度不能太高的原因是温度太高硝酸易分解
②步骤Ⅱ中发生反应:
4Fe(NO3)2+O2+(2n+4)H2O═24Fe2O3•H2O+8HNO3
4Fe+10HNO3═4Fe(NO3)2+NH4NO3+3H2O
第一个反应的氧化剂是O2
笫二个反应每生成1molNH4NO3,转移的电子数是8NA
③铁红可用于焊接钢轨,其反应的化学方程式为Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe
④上述生产结束后,流程中氮元素最主要的存在形式为b(填字母)
a.氮氧化物 b.硝酸按 c.硝酸亚铁 d.硝酸.
分析 (1)工业上用FeCl3溶液与铜发生氧化还原反应生成氯化亚铁和氯化亚铜这一原理来腐蚀印刷线路板;
(2)由流程图可知,Fe与硝酸反应生成硝酸亚铁,步骤Ⅱ中转化为Fe2O3•nH2O,最后得到铁红,
①硝酸受热易分解;
②根据反中的元素的化合价的变化判断氧化剂剂,根据电子得失守恒计算被还原的硝酸;
③铁红发生铝热反应,可用于焊接钢轨;
④根据流程图可知,生产结束后氮元素主要存在硝酸铵溶液中.
解答 解:(1)工业上用FeCl3溶液与铜发生氧化还原反应生成氯化亚铁和氯化亚铜这一原理来腐蚀印刷线路,反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)由流程图可知,Fe与硝酸反应生成硝酸亚铁,步骤Ⅱ中转化为Fe2O3•nH2O,最后得到铁红,
①硝酸受热易分解,所以步骤I温度不能太高,故答案为:温度太高硝酸易分解;
②在反应4Fe(NO3)2+O2+(2n+4)H2O═2Fe2O3•nH2O+8HNO3中,O元素的化合价从0价变为-2价,所以反应的氧化剂是O2,根据反应4Fe+10HNO3═4Fe(NO3)2+NH4NO3+3H2O可知,氮从+5价降到-3价,反应中共转移8个电子,所以每生成1molNH4NO3,转移8NA个电子,
故答案为:O2;8NA;
③铁红发生铝热反应,可用于焊接钢轨,其反应的化学方程式为Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,故答案为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;
④根据流程图可知,生产结束后氮元素主要存在硝酸铵溶液中,故答案为:b.
点评 本题考查较综合,涉及元素化合物的性质、物质的制备流程等,侧重分析能力及对基础知识应用能力的考查,把握化学反应原理及图象、流程的分析为解答的关键,题目难度中等.

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案| A. | 混合后溶液pH=7 | |
| B. | 所得混合溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 所得混合溶液中存在c(CH3COOH)+c(CH3COO-)=0.05molL-1 | |
| D. | 混合后溶液中存在c(Na+)+c(H+)=c(CH3COOH)+c(CH3COO-) |
| A. | 铝片跟氢氧化钠溶液反应 6H2O+2Al+2OH?═2[Al(OH)4]-+3H2↑ | |
| B. | 明矾溶液中加入过量的氨水 Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| C. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液 HCO3-+OH-═CO32-+2H2O | |
| D. | 铜片跟稀硝酸反应 Cu+NO3-+4H+═Cu2++NO↑+2H2O |
| A. | 配制一定物质的量浓度的硫酸溶液时,只需使用1次玻璃棒 | |
| B. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体时即停止加热 | |
| C. | 液溴盛放在用水液封的棕色试剂瓶中 | |
| D. | 用四氯化碳萃取碘的饱和水溶液中的碘.分液时显紫红色液体在下层 |
| A. | KClO3在反应中被还原 | |
| B. | 被还原与被氧化的氧元素的质量比为1:5 | |
| C. | H204在反应中既没被氧化也没被还原 | |
| D. | 生成1mol Cl2时有2mol电子转移 |
| A. | Fe与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 实验室制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 铜与稀硝酸反应:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
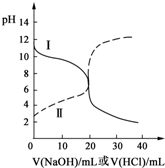 25℃时取浓度均为0.1000mol•L-1的CH3COOH(aq)和氨水各20mL,分别用0.1000mol•L-1NaOH(aq)、0.1000mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时取浓度均为0.1000mol•L-1的CH3COOH(aq)和氨水各20mL,分别用0.1000mol•L-1NaOH(aq)、0.1000mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A. | 曲线Ⅰ:滴加溶液到10.00mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | 曲线Ⅱ:滴加溶液到10.00mL时:c(CH3COO-)-c(CH3COOH)=2[c(OH-)-c(H+)] | |
| C. | 曲线Ⅱ:滴加溶液在10.00mL~20.00mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| D. | 曲线Ⅰ:滴加溶液到20.00mL时,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |