题目内容
1.用情性电极电解以下溶液,下列说法正确的是( )| A. | 电解NaOH溶液时,溶液浓度将增大,pH增大 | |
| B. | 电解H2SO4溶液时,溶液浓度将增大,pH增大 | |
| C. | 电解Na2SO4溶液时,溶液浓度将增大,pH不变 | |
| D. | 电解NaCl溶液时,溶液浓度将减小,pH不变 |
分析 A.用惰性电极电解NaOH溶液时,阴极上氢离子放电、阳极上氢氧根离子放电,相当于水解水,导致c(NaOH)增大;
B.电解稀硫酸时,阴极上氢离子放电、阳极上氢氧根离子放电,相当于水解水,导致硫酸浓度增大;
C.电解硫酸钠溶液时,阴极上氢离子放电、阳极上氢氧根离子放电,相当于水解水,导致硫酸钠浓度增大;
D.电解饱和NaCl溶液时,阴极上氢离子放电、阳极上氯离子放电,所以导致溶液中氯化钠浓度降低,但溶液中有NaOH生成.
解答 解:A.用惰性电极电解NaOH溶液时,阴极上氢离子放电、阳极上氢氧根离子放电,相当于水解水,导致c(NaOH)增大,溶液的pH增大,故A正确;
B.电解稀硫酸时,阴极上氢离子放电、阳极上氢氧根离子放电,相当于水解水,导致硫酸浓度增大,溶液的pH减小,故B错误;
C.电解硫酸钠溶液时,阴极上氢离子放电、阳极上氢氧根离子放电,相当于水解水,导致硫酸钠浓度增大,但硫酸钠是强酸强碱盐,其溶液呈中性,pH不变,故C正确;
D.电解饱和NaCl溶液时,阴极上氢离子放电、阳极上氯离子放电,所以导致溶液中氯化钠浓度降低,但溶液中有NaOH生成,溶液的pH增大,故D错误;
故选AC.
点评 本题考查电解原理,为高频考点,明确离子放电顺序、电解后溶液中溶质及其浓度变化是解本题关键,易错选项是C.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.化学与生活密切相关,下列应用中利用了物质氧化性的是( )
| A. | 明矾净化水 | B. | 用很稀的高锰酸钾溶液消毒 | ||
| C. | 食醋除水垢 | D. | 二氧化硫漂白草帽 |
9.无论在办公室还是居室里,在漂亮的花瓶中插上一束美丽的鲜花,将会给紧张而又忙碌的工作、生活带来轻松和愉悦的心情.如果在花瓶中加入“鲜花保鲜剂”,就会延长鲜花的寿命.
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是蔗糖(填写名称).
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林不含K+)$\frac{\frac{0.50}{174}×2+\frac{0.50}{158}}{V}$mol•L-1(只要求写表达式,不需计算).
(3)配制过程中,下列操作对配制结果没有影响的是AD(填字母).
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时俯视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有Cl-(填化学符号).
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林不含K+)$\frac{\frac{0.50}{174}×2+\frac{0.50}{158}}{V}$mol•L-1(只要求写表达式,不需计算).
(3)配制过程中,下列操作对配制结果没有影响的是AD(填字母).
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时俯视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)欲确定“鲜花保鲜剂”中硝酸银的浓度,则加入的试剂中应含有Cl-(填化学符号).
16.下列关于强、弱电解质的叙述错误的是( )
| A. | 强电解质在水溶液中完全电离成阴、阳离子 | |
| B. | 在溶液中,导电能力强的电解质是强电解质 | |
| C. | 纯净的强电解质在液态时,有的导电,有的不导电 | |
| D. | 对同一弱电解质来说,当溶液的温度和浓度不同时,其导电能力也不相同 |
6.有同学对三种牙膏中的摩擦剂成分进行调査,结果如下表:
试回答下列问题:
(1)上述三种摩擦剂中属于酸性氧化物的是SiO2(填化学式.下同);它与氢氟酸反应的
化学方程式是SiO2+4HF=SiF4↑+2H2O
(2)某品牌的摩擦剂可作胃酸中和剂,该反应的离子方程式为Al(OH)3+3H+=Al3++3H2O
(3)从摩擦剂成分考虑,向该防臭牙膏样品中滴加适量稀硝酸,该反应的化学方程式为CaCO3+2HNO3=CO2↑+H2O+Ca(NO3)2.
| 牙膏品牌 | 某儿童牙膏 | 某防臭牙膏 | 某透明牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)上述三种摩擦剂中属于酸性氧化物的是SiO2(填化学式.下同);它与氢氟酸反应的
化学方程式是SiO2+4HF=SiF4↑+2H2O
(2)某品牌的摩擦剂可作胃酸中和剂,该反应的离子方程式为Al(OH)3+3H+=Al3++3H2O
(3)从摩擦剂成分考虑,向该防臭牙膏样品中滴加适量稀硝酸,该反应的化学方程式为CaCO3+2HNO3=CO2↑+H2O+Ca(NO3)2.
11.甲、乙两个密闭容器中均发生反应:C(s)+2H2O(g)?CO2(g)+2H2(g)△H>0.有关实验数据如下表所示:
下列说法正确的是( )
容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | 平衡常数 | |
| C(s) | H2O(g) | H2(g) | |||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 3.5 | K1 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 | K2 |
| A. | T1<T2 | |
| B. | K2=1.35 mol•L-1(或K2=1.35) | |
| C. | 混合气体的密度始终保持不变 | |
| D. | 乙容器中,当反应进行到1.5 min时,n(H2O)=1.4 mol. |
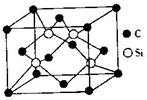 氮化硅是一种重要的结构陶瓷材料,具有优良性能.
氮化硅是一种重要的结构陶瓷材料,具有优良性能.