题目内容
4. 化工工业中常用乙苯脱氢的方法制备苯乙烯.
化工工业中常用乙苯脱氢的方法制备苯乙烯.已知某温度下:
反应①:CO2 (g)+H2(g)→CO(g)+H2O(g),△H=+41.2kJ/mol;
反应②:
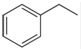 (g)→
(g)→ (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol;①②的化学反应平衡常数分别为K1、K2,
(1)①请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式CO2(g)+
 (g)+CO(g)+H2O(g) △H=+158.8 kJ/mol
(g)+CO(g)+H2O(g) △H=+158.8 kJ/mol②该反应的化学平衡常数K=K1•K2(用K1、K2表示)
(2)对于反应①,恒温恒容条件下,向密闭容器中加入2molCO2 和2molH2,当反应达到平衡后,以下说法正确的是B
( A) 因为该反应是吸热反应,所以升高温度,正反应速率增大,逆反应速率减小;
( B ) 若继续加入1molCO2、1mol H2,达到新平衡后CO2的体积分数不变;
( C ) 若继续通入1mol CO2则平衡向正反应方向移动,CO2的转化率增大;
( D) 压缩体积,平衡不移动,反应物和产物的浓度都不变;
(3)恒温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2;请在如图中画出t1之后的正逆反应曲线,并作出标注.
(4)已知某温度下,Ag2SO4的KspAg2SO4=0.36×10-6,向0.01mol•L-1的Na2SO4溶液中滴加AgNO3溶液至恰好有沉淀生成,此时AgNO3的浓度为6x10-3mol•L-1.
分析 (1)①根据盖斯定律,结合已知方程式计算反应热,然后写热化学方程式;
②方程式相加时,总平衡常数等于分方程的平衡常数之积;
(2)A、升高温度正逆反应速率均增大;
B、增大反应物,平衡正向移动;
C、若继续通入1mol CO2则平衡向正反应方向移动,CO2的转化率减小;
D、压缩体积,平衡不移动,反应物和产物的浓度都增大;
(3)恒温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2,则正反应速率瞬间增大,逆反应速率逐渐增大;
(4)根据Ag2SO4的KspAg2SO4=0.36×10-6进行计算.
解答 解:(1)①已知反应①:CO2(g)+H2(g)→CO(g)+H2O(g),△H=+41.2kJ/mol;
反应②: (g)→
(g)→ (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol;
根据盖斯定律:①+②,得 CO2(g)+ (g)+CO(g)+H2O(g)△H=+41.2+117.6=+158.8kJ/mol;
(g)+CO(g)+H2O(g)△H=+41.2+117.6=+158.8kJ/mol;
故答案为:CO2(g)+ (g)+CO(g)+H2O(g) △H=+158.8 kJ/mol;
(g)+CO(g)+H2O(g) △H=+158.8 kJ/mol;
②、反应①与法院②相加得总方程,则总方程的平衡常数等于分方程的平衡常数之积,即K=K1•K2;
故答案为:K1•K2;
(2)A、升高温度增大了活化分子百分数,有效碰撞几率增大,正逆反应速率均增大,故A错误;
B、若继续加入1mol CO2、1mol H2,与原平衡的初始量是等比例加入,反应物的浓度增大,则平衡向正反应方向移动,故B正确;
C、若继续通入1mol CO2,反应物的浓度增大,则平衡向正反应方向移动,由于平衡移动程度较小,CO2的转化率减小,故C错误;
D、该反应为总体积不变的反应,压缩体积,平衡不移动,但是反应物和产物的浓度都增大,故D错误;
故答案为:B;
(3)恒温恒容条件下,反应①达到平衡后;t1时刻通入少量CO2,则正反应速率瞬间增大,逆反应速率逐渐增大,其t1之后的正逆反应曲线为: ,故答案为:
,故答案为: ;
;
(4)设AgNO3的浓度为x,又知KspAg2SO4=0.36×10-6则:
x=$\sqrt{\frac{0.36×1{0}^{-6}}{0.01}}$=6×10-3,
故答案为:6×10-3.
点评 本题考查了热化学方程式的书写、平衡常数K的应用、影响速率及平衡的因素、Ksp的计算、电解原理的应用等,题目涉及的知识点较多,题目难度中等,侧重于考查学生对基础知识的综合应用能力.

| A. | 在放电时,正极发生的反应是Pb(s)+SO42-(aq)-2e-═PbSO4(s) | |
| B. | 在放电时,该电池的负极材料是铅板 | |
| C. | 在充电时,电池中硫酸的浓度不断变小 | |
| D. | 在充电时,阳极发生的反应是PbSO4(s)+2e-═Pb(s)+SO42-(aq) |
| A. | H2 | B. | AlCl3 | C. | CH4 | D. | H2SO4 |
(1)已知:2N2H4(1)+N2O4(1)═3N2(g)+4H2O(1)△H=-1225kJ•mol-1
断开1mol下列化学键吸收的能量分别为:N-H:391kJ;N-N:193kJ;N≡N:946kJ;O-H:463kJ.
则使1molN2O4(1)分子中化学键完全断裂时需要吸收的能量是1803KJ.
(2)t℃时,将一定量的NO2(g)和N2O4(g)充入一个容积为2L的恒容密闭容器中,浓度随时间变化关系如表所示:
| 时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/mol•L-1 | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/mol•L-1 | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
②前10min内用NO2表示的反应速率为0.04mol/(L•min),20min时改变的条件是增大NO2的浓度(或向容器中加入0.8mol二氧化氮);重新达到平衡时,NO2的百分含量与原平衡状态相比B(填序号)
A.增大 B.减小 C.不变 D.无法判断
(3)肼的性质与氨相似,其水溶液显弱碱性.请用电离方程式表示肼的水溶液显碱性的原因:N2H4+H2O?N2H+5+OH-.肼与氧气构成的燃料电池在碱性条件下放电时,生成水与一种无污染的气体.放电时,该电池负极的电极反应式为N2H4+4OH--4e-=4H2O+N2.
(4)已知在相同条件下N2H4•H2O的电离程度大于N2H5Cl的水解程度.常温下,若将0.2mo1•L-1N2H4•H2O溶液与0.1mol•L-1HCl溶液等体积混合,则溶液中N2H5+、Cl-、OH-、H+离子浓度由大到小的顺序为c(N2H5+)>c(Cl-)>c(OH-)>c(H+).
| A. |  | B. |  | C. |  | D. |  |
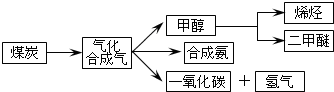
I.已知该产业链中某反应的平衡表达式为:K=$\frac{{c({H_2})•c({CO})}}{{c({H_2}O)}}$,它所对应反应的化学方程式为C(s)+H2O(g)?CO(g)+H2(g);
II.二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)?CH3OH(g)△H1=-90.7kJ•mol-1
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-23.5kJ•mol-1
③CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41.2kJ•mol-1
(1)催化反应室中总反应的热化学方程式为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H=-247kJ•mol-1,830℃时反应③的K=1.0,则在催化反应室中反应③的K>1.0(填“>”、“<”或“=”).
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H2)=2.4mol/L,5min后达到平衡,CO的转化率为50%,若反应物的起始浓度分别为:c(CO)=4mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2mol/L,a=5.4mol/L.
(3)反应②在t℃时的平衡常数为400,此温度下,在0.5L的密闭容器中加入一定量的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/(mol•L-1) | 0.8 | 1.24 | 1.24 |
②平衡时二甲醚的物质的量浓度是1.6mol/L.
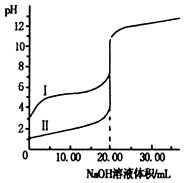 室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )
室温下,用0.1mol•L-1 NaOH溶液分别滴定20.00ml0.1mol•L-1的盐酸和醋酸溶液,滴定曲线如图.下列说法正确的是( )| A. | I、Ⅱ分别表示盐酸和醋酸的滴定曲线 | |
| B. | V(NaOH)=10.00mL时,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$>1 | |
| C. | pH=7时,两种酸所消耗NaOH溶液的体积相等 | |
| D. | V(NaOH)=20.00mL时,c(Cl一)<c(CH3COO一) |