题目内容
下列反应的离子方程式书写正确的是( )
| A、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
| B、稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| D、盐酸与氢氧化钠溶液反应:H++OH-=H2O |
考点:离子方程式的书写
专题:
分析:A.碳酸钙为难溶物,离子方程式中不能拆开,应该保留化学式;
B.稀硫酸与铁反应生成亚铁离子,不会生成铁离子;
C.氢氧化钡与稀硫酸反应除了生成硫酸钡沉淀,还生成水,漏掉了生成水的反应;
D.强酸盐酸与可溶性的强碱氢氧化钠反应生成可溶性的盐和水.
B.稀硫酸与铁反应生成亚铁离子,不会生成铁离子;
C.氢氧化钡与稀硫酸反应除了生成硫酸钡沉淀,还生成水,漏掉了生成水的反应;
D.强酸盐酸与可溶性的强碱氢氧化钠反应生成可溶性的盐和水.
解答:
解:A.碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故A错误;
B.稀硫酸与铁粉反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+=Fe2++H2↑,故B错误;
C.氢氧化钡溶液与稀硫酸反应生成硫酸钡和水,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.盐酸与氢氧化钠溶液反应生成氯化钠和水,反应的离子方程式为:H++OH-=H2O,故D正确;
故选D.
B.稀硫酸与铁粉反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+=Fe2++H2↑,故B错误;
C.氢氧化钡溶液与稀硫酸反应生成硫酸钡和水,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故C错误;
D.盐酸与氢氧化钠溶液反应生成氯化钠和水,反应的离子方程式为:H++OH-=H2O,故D正确;
故选D.
点评:本题考查了离子方程式的书写判断,是高考中的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等;选项B为易错点,注意反应产物为亚铁离子.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在200g浓度为18mol/L、密度为ρ(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,如果水的密度为1g/cm3则加入水的体积( )
| A、小于200mL |
| B、等于200mL |
| C、大于200mL |
| D、不能确定 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、22.4L氢气中含有氢分子的数目为NA |
| B、1 mol臭氧(O3)中含有氧原子的数目为2NA |
| C、常温常压下,14g氮气含有的原子数目为NA |
| D、0.5 mol/LFe2(SO4)3溶液中,SO42-的数目为1.5NA |
下列关于化学基本概念和基本理论的几点认识中正确的是( )
| A、胶体区别于其它分散系的本质特征是具有丁达尔现象 |
| B、根据化合物中含氢数目的多少,把化合物分为一元酸、二元酸、三元酸等 |
| C、碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 |
| D、强电解质溶液的导电能力一定强于弱电解质溶液 |
化学反应中,条件的有无对有些反应来说非常重要.例如,氯仿在正常情况下是一种良好的有机溶剂.能与乙醇、乙醚等多种有机溶剂互溶.但在高温、与明火或红热物体接触时,产生剧毒的光气、氯化氢等气体.光照在某些反应中也是极其重要的.在下列反应中,光照对反应几乎没有影响的是( )
| A、氯气与氢气的反应 |
| B、氯气与甲烷的反应 |
| C、氟气与氢气的反应 |
| D、次氯酸的分解 |
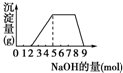 某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随加入的溶液中NaOH的物质的量的变化如图所示:[已知:Mg2++2OH-═Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓,且Mg(OH)2、Fe(OH)3难溶于水;NH4++OH-═NH3?H2O]由此可知,该溶液中肯定含有的离子是
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随加入的溶液中NaOH的物质的量的变化如图所示:[已知:Mg2++2OH-═Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓,且Mg(OH)2、Fe(OH)3难溶于水;NH4++OH-═NH3?H2O]由此可知,该溶液中肯定含有的离子是