题目内容
7.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )| A. | 常温下1LpH=11的氨水中含有阳离子总数为0.001NA | |
| B. | 4g${\;}_{1}^{2}$H2中所含的质子数为4NA | |
| C. | 1mol甲醇中含有C-H键的数目为4NA | |
| D. | 常温常压下,22.4L的NO2和CO2混合气体含有2NA个氧原子 |
分析 A、pH=11的氨水中,氢氧根的浓度为0.001mol/L,根据电荷守恒来分析;
B、求出重氢的物质的量,然后根据1mol重氢中含2mol质子来分析;
C、甲醇中含3条C-H键;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答 解:A、pH=11的氨水中,氢氧根的浓度为0.001mol/L,根据电荷守恒可知:c(OH-)=c(H+)+c(NH4+),故溶液中的阳离子的浓度和为0.001mol/L,故溶液中的阳离子的个数和为0.001NA个,故A正确;
B、4g重氢的物质的量为1mol,而1mol重氢中含2mol质子,故含2NA个,故B错误;
C、甲醇中含3条C-H键,故1mol甲醇中含3NA个C-H键,故C错误;
D、常温常压下,气体摩尔体积大于22.4L/mol,故混合气体的物质的量小于1mol,则含有的氧原子的个数小于2NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
17.下列叙述正确的是( )
| A. | 硫酸可以用于除去锅炉或水壶中的水垢 | |
| B. | 切开的苹果放置后变色和纸张久置后变黄的原理相同 | |
| C. | 蜂蚁蛰咬人时会向人体注入酸性物质,可涂抹小苏打溶液缓解疼痛 | |
| D. | 工业含酸废水可用氢氧化钡溶液处理后再排放,有利于减少水体污染 |
15.下列分子中,所有原子不可能处在同一平面上的是( )
| A. | CH4 | B. | CS2 | C. | H2O | D. | SO2 |
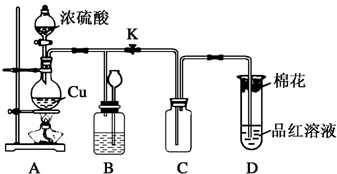
2.利用右图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀盐酸 | MnO2 | 石蕊溶液 | 石蕊溶液先变红后褪色 | |
| B | 浓硫酸 | 蔗糖 | 品红 | 浓硫酸有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | 生成BaSO3白色沉淀 | |
| D | 醋酸 | Na2CO3 | 苯酚钠溶液 | 酸性:醋酸>碳酸>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
12. X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:①X元素原子价电子排布式为ns2np3,且原子半径是同族元素中最小的.②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子.③Z元素的电离能数据如表(kJ/mol):
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:①X元素原子价电子排布式为ns2np3,且原子半径是同族元素中最小的.②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子.③Z元素的电离能数据如表(kJ/mol):
请回答:
(1)Z2Y2的电子式为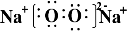 ,含有的化学键类型为离子键、非极性键,Z2Y2为离子晶体、
,含有的化学键类型为离子键、非极性键,Z2Y2为离子晶体、
(2)Z2Y2遇水发生强烈水解产生一种气体A,溶液呈碱性,则A的结构式为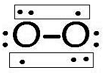 ,其分子空间构型为直线型.
,其分子空间构型为直线型.
(3)X、Y、Z、W四种元素所形成的单质中,硬度最大的是金刚石(填物质的名称);晶体ZW的熔点比晶体XW4明显高的原因是NaCl为离子晶体而CCl4为分子晶体;XW4中X原子的杂化轨道类型为sp3.
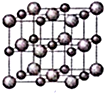
(4)ZW晶体的结构示意图如图所示.设该晶体的摩尔质量为M g/mol,晶体的密度为ρ g/cm3.阿伏伽德罗常数为NA,则晶体中两个最近的Z离子中心间的距离=$\frac{\sqrt{2}}{2}$$\root{3}{\frac{4M}{ρ{N}_{A}}}$.
 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:①X元素原子价电子排布式为ns2np3,且原子半径是同族元素中最小的.②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子.③Z元素的电离能数据如表(kJ/mol):
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:①X元素原子价电子排布式为ns2np3,且原子半径是同族元素中最小的.②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子.③Z元素的电离能数据如表(kJ/mol):| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
(1)Z2Y2的电子式为
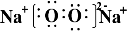 ,含有的化学键类型为离子键、非极性键,Z2Y2为离子晶体、
,含有的化学键类型为离子键、非极性键,Z2Y2为离子晶体、(2)Z2Y2遇水发生强烈水解产生一种气体A,溶液呈碱性,则A的结构式为
 ,其分子空间构型为直线型.
,其分子空间构型为直线型.(3)X、Y、Z、W四种元素所形成的单质中,硬度最大的是金刚石(填物质的名称);晶体ZW的熔点比晶体XW4明显高的原因是NaCl为离子晶体而CCl4为分子晶体;XW4中X原子的杂化轨道类型为sp3.
(4)ZW晶体的结构示意图如图所示.设该晶体的摩尔质量为M g/mol,晶体的密度为ρ g/cm3.阿伏伽德罗常数为NA,则晶体中两个最近的Z离子中心间的距离=$\frac{\sqrt{2}}{2}$$\root{3}{\frac{4M}{ρ{N}_{A}}}$.
19.已烯雌酚是一种激素类药物,结构如下:
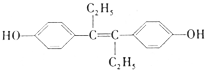
下列有关叙述中不正确的是( )

下列有关叙述中不正确的是( )
| A. | 可以用有机溶剂萃取 | |
| B. | 可与NaOH或NaHCO3溶液发生反应 | |
| C. | 1mol该有机物可以与5molBr2发生反应 | |
| D. | 该有机物分子中,可能有8个碳原子共平面 |
16.下列物质中,既含共价键又含离子键的是( )
| A. | NaCl | B. | O2 | C. | NaOH | D. | CO2 |
 .
. .
.