题目内容
6.有下列物质:①O2 ②Na2O2 ③NaOH ④CO2 ⑤H2O2 ⑥CaCl2 ⑦NH4Cl(1)含有离子键构成的物质是②③⑥⑦.
(2)只由非极性键构成的物质是①.
(3)由极性键和非极性键构成的物质是⑤.
(4)由离子键和极性键构成的物质是③.
(5)由离子键和非极性键构成的物质是②.
分析 一般来说,活泼金属与非金属形成离子键,非金属元素之间形成共价键,不同非金属形成极性键,同种非金属形成非极性键,以此来解答.
解答 解:①O2 中只含非极性键;
②Na2O2中含离子键和O-O非极性键;
③NaOH含离子键和O-H极性键;
④CO2只含C、O之间的极性键;
⑤H2O2中含O-H极性键和O-O非极性键;
⑥CaCl2中只含离子键;
⑦NH4Cl中含离子键和N-H极性键,则
(1)含有离子键构成的物质是②③⑥⑦,故答案为:②③⑥⑦;
(2)只由非极性键构成的物质是①,故答案为:①;
(3)由极性键和非极性键构成的物质是⑤,故答案为:⑤;
(4)由离子键和极性键构成的物质是③,故答案为:;
(5)由离子键和非极性键构成的物质是②,故答案为:②.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.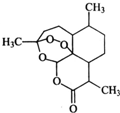 中国女科学家屠呦呦因为发现青蒿素获颁诺贝尔医学奖.图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )
中国女科学家屠呦呦因为发现青蒿素获颁诺贝尔医学奖.图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )
 中国女科学家屠呦呦因为发现青蒿素获颁诺贝尔医学奖.图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )
中国女科学家屠呦呦因为发现青蒿素获颁诺贝尔医学奖.图是青蒿素的结构,则有关青蒿素的说法中不正确的是( )| A. | 有“-O-”键,分子式C15H22O5,可发生取代反应 | |
| B. | 有“六元环”结构,是苯的同系物,可发生加成反应 | |
| C. | 有“-O-O-”键,氧化性较强,可发生还原反应 | |
| D. | 有“-COOC-”键,碱性条件下,可发生水解反应 |
3.下列描述中正确的是( )
| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | CO32-VSEPR模型名称与离子的立体构型名称不一致 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
20.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 0.1mol•L-1的NaCl溶液中Cl-的数目为0.1NA | |
| B. | 16g O2和O3的混合气体中所含的氧原子数为NA | |
| C. | 22.4L H2中含有的氢原子数一定为2NA | |
| D. | 1mol Cl2与过量的金属钠充分反应后,转移的电子数为NA |
1.现有苯甲酸、苯酚溶于乙醇所得的混合液,某同学设计方案分离三种物质,并检验其中的某些离子和物质.
已知:(1)酸性强弱:HCl>苯甲酸>H2CO3>苯酚>HCO3-
(2)部分物理参数如下:
供选择试剂:10%氢氧化钠溶液、0.1mol/L盐酸、0.1mol/LNa2CO3、0.1mol/L NaHCO3、浓溴水、生石灰、0.1mol/L FeCl3、0.1mol/L BaCl2、CO2、0.1mol/L溴水、澄清石灰水
(1)分离物质流程如下:
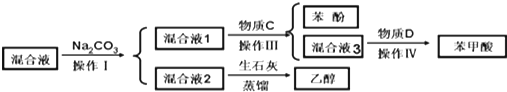
物质C是CO2,操作IV是过滤.
(2)操作III发生的主要化学反应方程式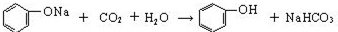 .
.
(3)混合液2中加入生石灰的原因是生石灰与混合液2中的水反应,生成氢氧化钙溶液,并放出热量,便于乙醇从混合物中蒸馏出.
(4)该同学检验混合液1中是否含有苯酚和NaHCO3,以证明酸性的强弱.完成下列各步实验及实验现象和结论.
(5)称取2.0g苯甲酸和苯酚的混合固体溶于足量乙醇中,滴加足量饱和NaHCO3溶液,测得放出的CO2(标准状况下,不考虑CO2溶于水)为33.6mL,则苯甲酸的质量分数为$\frac{\frac{0.036L}{22.4L/mol}×122g/mol}{2g}$×100%,(只列式,不计算),结果为9.2%.(结果保留1位小数)(苯甲酸的相对分子质量为122,苯酚相对分子质量为94)
已知:(1)酸性强弱:HCl>苯甲酸>H2CO3>苯酚>HCO3-
(2)部分物理参数如下:
| 密度 (g•mL-1) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 苯甲酸 | 1.2659 | 122.13 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
| 苯酚 | 1.07 | 40.6 | 181.9 | 易溶于乙醇、乙醚,65℃以上能与水互溶 |
| 乙醇 | 0.79 | -114.3 | 78.5 | 与水混溶,可混溶于醚、氯仿、甘油等多数有 机溶剂 |
(1)分离物质流程如下:

物质C是CO2,操作IV是过滤.
(2)操作III发生的主要化学反应方程式
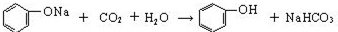 .
.(3)混合液2中加入生石灰的原因是生石灰与混合液2中的水反应,生成氢氧化钙溶液,并放出热量,便于乙醇从混合物中蒸馏出.
(4)该同学检验混合液1中是否含有苯酚和NaHCO3,以证明酸性的强弱.完成下列各步实验及实验现象和结论.
| 实验步骤 | 现象和结论 |
| ①取少量混合液1于试管,滴加BaCl2, 振荡,静置 | 产生白色沉淀,BaCO3 |
| ②取少量步骤①上层清夜于试管,滴加0.1mol/L盐酸再将产生的气体通入澄清石灰水中 | 澄清石灰水变浑浊 说明混合液1含有HCO3- |
| ③另取少量混合液1于试管,滴加0.1mol/L FeCl3溶液,振荡 | 溶液不显紫色, 说明混合液1不含有酚羟基 |
11.An+、Bn-、C 3种短周期元素的粒子具有相同的电子层结构,则关于它们的叙述正确的是( )
| A. | 原子序数:C>B>A | B. | 离子半径:Bn-<An+ | ||
| C. | C是稀有气体元素的原子 | D. | 原子半径:A<B |

 ,
, +CO2+H2O→
+CO2+H2O→ +NaHCO3,
+NaHCO3, +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O.