题目内容
将等物质的量的H2和I2充入体积为2L的密闭容器中,进行反应:H2(g)+I2(g)?2HI(g),测得2min内v (HI)=0.1mol?L-1?min-1,2min 后I2(g)的浓度为0.4mol?L-1,试确定:
(1)2min内以H2所表示的反应速率为 ;
(2)I2的起始物质的量为 ;
(3)2min末HI的浓度为 .
(1)2min内以H2所表示的反应速率为
(2)I2的起始物质的量为
(3)2min末HI的浓度为
考点:化学平衡的计算
专题:
分析:(1)同一可逆反应中同一时间段内,各物质的反应速率之比等于其计量数之比,从而计算氢气、碘的反应速率;
(2)根据△c=vt计算参加反应的碘的物质的量浓度,H2和I2的起始浓度=2min末碘蒸气浓度+参加反应的碘蒸气浓度;
(3)HI为生成物,根据△c=vt计算出2min末HI的浓度.
(2)根据△c=vt计算参加反应的碘的物质的量浓度,H2和I2的起始浓度=2min末碘蒸气浓度+参加反应的碘蒸气浓度;
(3)HI为生成物,根据△c=vt计算出2min末HI的浓度.
解答:
解:(1)同一可逆反应中同一时间段内,各物质的反应速率之比等于其计量数之比,所以H2的反应速率为v(H2)=
v(HI)=
×0.1mol?(L?min)-1=0.05mol?(L?min)-1,
故答案为:0.05mol?(L?min)-1;
(2)参加反应的碘蒸气浓度:△c(I2)=vt=0.05mol/(L.min)×2min=0.1mol/L,碘蒸气的起始浓度为:c(I2)=0.1mol/L+0.4mol/L=0.5mol/L;
氢气和碘单质的物质的量相等,则起始浓度:c(H2)=c(I2)=0.5mol/L,物质的量为×2L=1mol,
故答案为:1mol;
(3)HI为生成物,测得2min时v(HI)=0.1mol?(L?min)-1,则2min时生成HI的物质的量浓度为:c(HI)=0.1mol?(L?min)-1×2min=0.2 mol?L-1,
故答案为:0.2mol?L-1.
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:0.05mol?(L?min)-1;
(2)参加反应的碘蒸气浓度:△c(I2)=vt=0.05mol/(L.min)×2min=0.1mol/L,碘蒸气的起始浓度为:c(I2)=0.1mol/L+0.4mol/L=0.5mol/L;
氢气和碘单质的物质的量相等,则起始浓度:c(H2)=c(I2)=0.5mol/L,物质的量为×2L=1mol,
故答案为:1mol;
(3)HI为生成物,测得2min时v(HI)=0.1mol?(L?min)-1,则2min时生成HI的物质的量浓度为:c(HI)=0.1mol?(L?min)-1×2min=0.2 mol?L-1,
故答案为:0.2mol?L-1.
点评:本题考查了化学平衡、化学反应速率的计算,题目难度中等,注意掌握化学反应速率与化学计量数的关系,明确化学反应速率的概念及计算方法,试题侧重考查了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
能在水溶液中大量共存的一组离子是( )
| A、K+、SO42-、Cu2+、NO3- |
| B、Ag+、Fe3+、Cl-、SO42- |
| C、H+、I-、NO3-、SiO32- |
| D、NH4+、OH-、Cl-、HCO3- |
某同学设计了以下流程来检验碳酸钾粉末中含有少量氯化钾和氢氧化钾.下列说法不正确的是( )
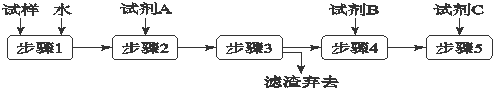

| A、步骤3的操作名称是过滤 |
| B、步骤1所需玻璃仪器是烧杯和玻璃棒 |
| C、试剂A是BaCl2溶液 |
| D、加入试剂A 的目的是除去CO32-并避免对Cl-或OH-的检验的干扰 |
关于如图所示的装置,不正确的说法是( )
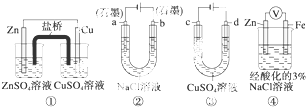

| A、装置①中,电池反应为Zn+Cu2+═Zn2++Cu |
| B、装置②工作一段时间后,a极附近溶液的pH增大 |
| C、用装置③精炼铜时,d极为粗铜 |
| D、装置④中电子由Zn流向Fe,Na+、H+移向Zn电极 |
下列叙述错误的是( )
| A、将CO2通入BaCl2溶液中至饱和,有沉淀产生 |
| B、在NaHCO3溶液中,加入澄清石灰水,有白色沉淀生成 |
| C、向AlCl3溶液中滴加浓氨水,产生白色沉淀;再加入过量浓氨水,沉淀仍不消失 |
| D、向FeCl2溶液中滴入KSCN溶液没有现象,再滴入氯水溶液变红 |