题目内容
5.工业上生产乙烯的原料是( )| A. | 溴乙烷 | B. | 天然气 | C. | 石油 | D. | 酒精 |
分析 A.溴乙烷发生消去反应能生成乙烯;
B.天然气的主要成分为甲烷;
C.石油裂解得到乙烯;
D.酒精发生消去反应生成乙烯.
解答 解:天然气不能生成乙烯,溴乙烷、酒精能发生消去反应生成乙烯,但不能用于工业生产,则工业上生产乙烯的原料为石油,
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握物质的性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意工业生产的限制,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列对某些问题的认识正确的是( )
| A. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| B. | 在船底镶嵌锌块和将船体与电源负极相连,二者防腐的方法都称为牺牲阳极的阴极保护法 | |
| C. | 1 mol葡萄糖水解能生成2mol CH3CH2OH和2mol CO2 | |
| D. | 不能用带玻璃塞的玻璃瓶和酸式滴定管盛取碱液,二者的原因是相同的 |
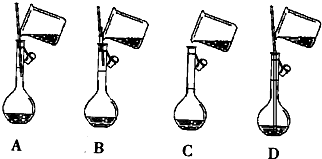
14.实验时遇到下列情况,将使所配溶液的浓度偏高的是 ( )
| A. | 在配制前用稀硫酸润洗容量瓶后,未用蒸馏水洗涤 | |
| B. | 定容摇匀后,发现液面低于刻度线,再加入蒸馏水至与刻度线相切 | |
| C. | 洗涤量筒,并将洗涤液转入容量瓶 | |
| D. | 定容时仰视读数. |
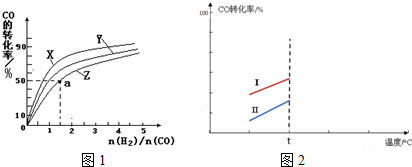
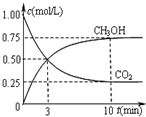 工业上可以以煤和水为原料通过一系列转化变为清洁能源氢气或工业原料甲醇.
工业上可以以煤和水为原料通过一系列转化变为清洁能源氢气或工业原料甲醇.
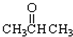 ③CH3CH2Br ④
③CH3CH2Br ④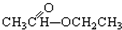 ⑤
⑤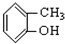 ⑥
⑥ ⑦
⑦ ⑧
⑧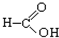 ⑨
⑨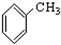 ⑩
⑩