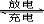题目内容
用吸收H2后的稀土储氢合金作为电池负极材料(用MH表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池.电池充放电时的总反应为:NiO(OH)+MH
Ni(OH)2+M,下列叙述不正确的是( )
| 放 |
| 充 |
分析:NiO(OH)+MH
Ni(OH)2+M,放电为原电池,充电为电解,放电时Ni元素的化合价降低,MH为负极材料,元素的化合价升高,充电时正极与阳极相连,以此来解答.
| 放 |
| 充 |
解答:解:A.电池放电时,负极元素的化合价升高,发生氧化反应,故A正确;
B.放电时,阴离子向负极移动,则电解质溶液中的OH-移向负极,故B正确;
C.充电时在阳极发生氧化反应,电极反应为为Ni(OH)2-e-+OH-=NiO(OH)+H2O,故C正确;
D.充电完成时M全部转化为MH,该阴极只能为氢离子放电生成氢气,不会生成氧气,故D错误;
故选D.
B.放电时,阴离子向负极移动,则电解质溶液中的OH-移向负极,故B正确;
C.充电时在阳极发生氧化反应,电极反应为为Ni(OH)2-e-+OH-=NiO(OH)+H2O,故C正确;
D.充电完成时M全部转化为MH,该阴极只能为氢离子放电生成氢气,不会生成氧气,故D错误;
故选D.
点评:本题考查原电池和电解池原理,明确电池反应中元素的化合价变化及工作原理即可解答,注意与氧化还原反应的结合,题目难度不大.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目