��Ŀ����
 ij����С������ͼ��ʾװ�ý���ʵ�飮ʵ������У������������������Y������Һ����Ϻ�ɫ��ֹͣʵ�飬���缫���Ա�ϸ�����Һ��Ȼ���壮�������Ϸ��֣��������
ij����С������ͼ��ʾװ�ý���ʵ�飮ʵ������У������������������Y������Һ����Ϻ�ɫ��ֹͣʵ�飬���缫���Ա�ϸ�����Һ��Ȼ���壮�������Ϸ��֣��������FeO2-4������Һ�г��Ϻ�ɫ��
��1���������У�X������Һ��pH
��2���������У�Y�������ĵ缫��ӦΪ4OH--4e-=2H2O+O2����
��3������X���ռ���672mL���壬��Y���ռ���168mL���壨��������Ϊ��״��ʱ�������������Y�缫�����缫����������
��4���ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4+3Zn�TFe2O3+ZnO+2K2ZnO2���õ�����������ĵ缫��ӦʽΪ
���㣺���ԭ��
ר�⣺�绯ѧר��
��������1���������У�X�缫��H+�ŵ�����������ͬʱ�缫������OH-���ɣ�
��2��Y�缫�ϻ������ķ�ӦΪFeʧ���Ӻ����������ӷ�Ӧ���ɸ���������Ӻ�ˮ��
��3������ת�Ƶ�����ȼ������ܽ��������
��4�������ϸ���������ӵõ��Ӻ�ˮ��Ӧ���������������������ӣ�
��2��Y�缫�ϻ������ķ�ӦΪFeʧ���Ӻ����������ӷ�Ӧ���ɸ���������Ӻ�ˮ��
��3������ת�Ƶ�����ȼ������ܽ��������
��4�������ϸ���������ӵõ��Ӻ�ˮ��Ӧ���������������������ӣ�
���
�⣺��1���������У�X�缫�ϵ缫��ӦʽΪ2H2O+2e-=H2��+2OH-������c��OH-��������Һ��pH���ʴ�Ϊ������
��2��Y�缫�ϻ������ķ�ӦΪFeʧ���Ӻ����������ӷ�Ӧ���ɸ���������Ӻ�ˮ���缫��ӦʽΪFe-6e-+8OH-=FeO42-+4H2O���ʴ�Ϊ��Fe-6e-+8OH-=FeO42-+4H2O��
��3��X�缫�ռ���������������n��H2��=
=0.03mol��Y�缫�������������ʵ���=
=0.0075mol������ת�Ƶ�����ȵ����ܽ������=
��56g/mol=0.28g���ʴ�Ϊ��0.28��
��4�������ϸ���������ӵõ��Ӻ�ˮ��Ӧ���������������������ӣ��缫��ӦʽΪ2FeO42-+6e-+5H2O=Fe2O3+10OH-���ʴ�Ϊ��2FeO42-+6e-+5H2O=Fe2O3+10OH-��
��2��Y�缫�ϻ������ķ�ӦΪFeʧ���Ӻ����������ӷ�Ӧ���ɸ���������Ӻ�ˮ���缫��ӦʽΪFe-6e-+8OH-=FeO42-+4H2O���ʴ�Ϊ��Fe-6e-+8OH-=FeO42-+4H2O��
��3��X�缫�ռ���������������n��H2��=
| 0.672L |
| 22.4L/mol |
| 0.168L |
| 22.4L/mol |
| 0.03mol��2-0.0075mol��4 |
| 6 |
��4�������ϸ���������ӵõ��Ӻ�ˮ��Ӧ���������������������ӣ��缫��ӦʽΪ2FeO42-+6e-+5H2O=Fe2O3+10OH-���ʴ�Ϊ��2FeO42-+6e-+5H2O=Fe2O3+10OH-��
���������⿼���˵��ԭ������ȷ�������Ƶ���ȡԭ���ǽⱾ��ؼ����ٽ��ת�Ƶ�����Ƚ����йؼ��㣬�ѵ��ǵ缫��Ӧʽ��д����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
��֪NA���������ӵ�����������˵����ȷ���ǣ�������
| A��34g H2O2�к��е���������ΪNA |
| B��1mol�ؼ���-CD3�����е�����Ϊ9NA |
| C���ں�Al3+����ΪNA��AlCl3��Һ�У�Cl-����Ϊ3NA |
| D��1mol���������������ϡ���ᷴӦʱ��ת�Ƶ�������3NA |
����˵���У�������ǣ�������
| A��λ��ͬһ���ڵ�Ԫ��ԭ�Ӿ�����ͬ�ĵ��Ӳ��� |
| B��λ��ͬһ�����Ԫ��ԭ�Ӿ�����ͬ������������ |
| C��IA��Ԫ��ԭ�ӵ�������Ӳ㶼ֻ��1�����ӣ�����IA��Ԫ�ؾ�Ϊ���ý���Ԫ�� |
| D��ϡ������Ԫ�����ڵ����Ϊ0�壬��ԭ�ӵ�������Ӳ㲻��Ϊ8���ӽṹ |
����װ���ܹ����ԭ��ز�����ԭ��ط�Ӧ���ǣ�������
A�� ϡ���� |
B�� ϡ���� |
C��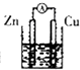 ����ͭ |
D�� �Ҵ� |
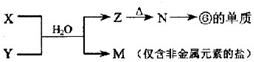
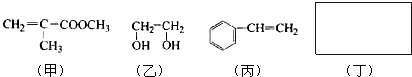
 ����������Ϣ���Ա�����ϩ���Ȼ���Ϊԭ�Ͼ�������Ӧ�ϳɱ�����������ȡ����Ӧ�Ļ�ѧ����ʽ��
����������Ϣ���Ա�����ϩ���Ȼ���Ϊԭ�Ͼ�������Ӧ�ϳɱ�����������ȡ����Ӧ�Ļ�ѧ����ʽ��