题目内容
在固定容积的容器中盛有1mol PCl5,200℃时发生如下反应:PCl5(g)?PCl3+Cl2(g)达到平衡时,PCl5体积分数为M%.若在同一温度和同一容器中,最初投入2molPCl5,达平衡时,PCl5所占体积分数为N%,则M和N的关系是( )
| A、M<N | B、M>N |
| C、M=N | D、无法比较 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:该反应是气体体积增大的化学反应,增大压强,平衡向逆反应方向移动,根据压强对化学平衡的影响分析.
解答:
解:根据PV=nRT知,R为常数,当V、T相同时,n越大,P越大;该反应是气体体积增大的反应,当投入的物质的量加倍时,则相当于增大压强,平衡向气体体积减小的方向移动,即逆反应方向移动,所以导致反应达到平衡时PCl5的转化率减小,PCl5的体积分数增大,故M<N.
故选A.
故选A.
点评:本题考查了外界条件对化学平衡的影响,难度中等,正确运用等效平衡是解本题的关键.

练习册系列答案
相关题目
下列操作达不到预期目的是( )
①将某卤代烃与氢氧化钠的水溶液共热,向冷却后的反应液中滴加AgNO3溶液,若产生白色沉淀,则证明该卤代烃为氯代烃
②用乙醇和30%的硫酸共热到170℃制取乙烯
③在少量苯酚稀溶液中滴入过量饱和溴水出现白色沉淀
④将苯与浓硝酸混合加热至60℃制备硝基苯
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,再加入银氨溶液加热.
①将某卤代烃与氢氧化钠的水溶液共热,向冷却后的反应液中滴加AgNO3溶液,若产生白色沉淀,则证明该卤代烃为氯代烃
②用乙醇和30%的硫酸共热到170℃制取乙烯
③在少量苯酚稀溶液中滴入过量饱和溴水出现白色沉淀
④将苯与浓硝酸混合加热至60℃制备硝基苯
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,再加入银氨溶液加热.
| A、①③④ | B、②③⑤ |
| C、①②④⑤ | D、①②③④⑤ |
下列各装置中铜电极上能产生气泡的是( )
A、 |
B、 |
C、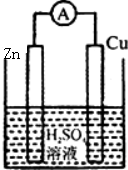 |
D、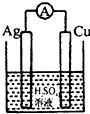 |
下列实验操作正确的是( )
A、 干燥Cl2 干燥Cl2 |
B、 制氢氧化亚铁 制氢氧化亚铁 |
C、 碳酸氢钠受热分解 碳酸氢钠受热分解 |
D、 检查容量瓶是否漏水 检查容量瓶是否漏水 |
常温下,0.1mol/L NH3?H2O溶液中存在如下电离平衡:NH3?H2O?NH4++OH-下列叙述正确的是( )
| A、加入少量NaOH固体,平衡正向移动 |
| B、加入少量水稀释,溶液中c(H+)减小 |
| C、加入少量MgSO4固体,溶液pH减小 |
| D、加入少量NH4Cl固体,平衡正向移动,Kb不变 |
25℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A、pH=3的盐酸中:c(H+)=3.0mol?L-1 |
| B、0.1mol?L-1的碳酸钠溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol?L-1 |
| C、氯化铵溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、碳酸氢钠溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
下列各图有关量的变化趋势中错误的是( )
A、 图为向盐酸中滴加NaOH发生中和反应过程中溶液温度的变化趋势 |
B、 图为向醋酸中滴加NaOH发生中和反应过程中各物质浓度的变化趋势 |
C、 图中能量≥Ec的分子称为活化分子,E为分子平均能量,则活化能为Ec-E |
D、 图为未加入催化剂和加入催化剂的反应进程中的能量变化 |
